Азот содержащие продукты
где его больше всего, список продуктов питания, богатых данным элементом
Азот входит в состав земной атмосферы в молекулярном виде, на него приходится 76% атмосферы по массе.
В связанном состоянии элемент встречается в почве и воде в виде химических соединений.
В живых организмах (растениях и животных) азот представлен в составе органических соединений, входит в аминокислоты в количестве от 15% до 18%.
к оглавлению ↑Как влияет на организм
В начале 20 века было установлено, что для обеспечения жизнедеятельности живых организмов необходимо регулярное поступление в них некоторых химических соединений, включая азот.

В теле мужчины содержится в среднем 1,8 кг элемента, а женщины – 1,3 кг. Такая разница обусловлена тем, что белки входят в состав мышечной ткани, а у мужчин мышцы развиты сильнее, чем у женщин.
Для человека атмосферный азот является биологически неактивным веществом, поступающим в легкие с вдыхаемым воздухом и выводимым с выдыхаемым.
Потребность человека в белке складывается из 2 компонентов – удовлетворение потребности в общем азоте и в незаменимых аминокислотах.
Белковые соединения для синтеза своих тканей человек получает из пищи, которая должна содержать достаточное их количество.
Из необходимых организму аминокислот некоторые (называемые заменимыми) синтезируются в организме из аммиака и иных веществ, а несинтезируемые (называемые незаменимыми) должны поступать с пищей (растительной и животной).
Чтобы атмосферный азот оказался в составе белков, он должен претерпеть ряд превращений. Использовать его напрямую способны лишь живущие в почве бактерии рода Азотобактер с дальнейшим синтезом органических азотистых соединений.
Все остальные живые организмы не способны использовать атмосферный азот. У них азотистый обмен начинается с использования аммиака или аминокислот.
Аммиак образуют высшие растения путем восстановления содержащихся в почве нитратов с конечным биосинтезом аминокислот и белков.
Травоядные животные питаются растениями и превращают аминокислоты растений в собственные белки. Человек потребляет растительные и животные продукты и также превращает их в собственные ткани.
После смерти живых организмов микроорганизмы расщепляют органические вещества, азот поступает в почву, где ассимилируется азотфиксирующими бактериями и вновь превращается в органические вещества. Это и есть кругооборот азота в природе.
к оглавлению ↑Потребность человека в белке, симптомы дефицита
В конце 19 века было окончательно установлено, что при нормальных условиях организм человека находится в состоянии азотистого равновесия, т. е. поступление азота с пищей равняется количеству элемента в выделяемых с мочой азотистых веществах (мочевине).

Количество выделяемой взрослым человеком мочевины зависит от количества потребляемой белковой пищи и обычно составляет 25-35 г в сутки.
Азотистый баланс нарушается при голодании или недостатке в пище белков. Длительное состояние отрицательного азотистого баланса (когда азота выводится больше, чем поступает) ведет к гибели организма.
Положительный азотистый баланс наблюдается в период восстановления после голодания или истощения. Нормальным является положительный азотистый баланс у растущих детей и подростков до периода прекращения их роста.
Для поддержания азотистого равновесия человеку, по нормам Всемирной организации здравоохранения, достаточно потреблять ежесуточно 0,8 г полноценного по аминокислотному составу белка на каждый килограмм своего веса.
При смешанном растительно-животном питании потребность в связи со снижением усвояемости возрастает и доходит до 1,0 г/кг. Под весом при данном расчете понимается нормальный (идеальный) вес без учета избыточной жировой ткани, например, по формуле «Рост минус 105».
При перечисленных ниже состояниях потребность в белке (и в азоте) увеличивается:
- стрессы;
- заболевания и травмы;
- после хирургических операций;
- беременность;
- грудное вскармливание;
- интенсивная физическая нагрузка.

При избыточном весе и похудении на сниженном по калорийности рационе также необходимо увеличить норму белка до 1,2-1,3 г/кг.
Но здесь нужна мера – потребление белка в количестве свыше 1,5 г/кг нежелательно, а свыше 2 г/кг — вредно.
Рекомендации по потреблению больших доз отдельных аминокислот или их комбинаций в виде добавки для спортсменов силовых видов спорта и бодибилдеров не подтверждаются, а применение чистых аминокислот считается неблагоприятным для здоровья, тем более, если они поступают взамен белковой пищи.
В чистом виде белковая недостаточность встречается редко. Это следствие общего недоедания, т. е. недостаточности калорийности рациона. Состояние при одновременном глубоком дефиците белка и энергии называется маразмом.
К социальным причинам недостаточности питания относятся:
- стихийные бедствия;
- войны;
- терроризм.
Поражает белково-энергетическая недостаточность беднейшие слои населения.
В развитых странах белково-калорийная недостаточность может наступать, как следствие заболеваний, хронического алкоголизма и наркомании, со снижением потребления пищи и нарушением ее усвоения.
Симптомы белково-калорийной недостаточности:
- задержка роста детей;
- слабость и потеря мышечной массы, что ведет к снижению веса тела;
- развитие обширных отеков;
- сухость и шелушение кожных покровов;
- образование медленно заживающих гноящихся язв;
- выпадение и обесцвечивание волос;
- потеря аппетита, тошнота;
- рвота с последующим обезвоживанием;
- анемия;
- снижение иммунитета.

Где его содержание больше всего, рекомендации по употреблению
Наиболее полноценные по аминокислотному составу белки содержатся в животных продуктах – мясе, рыбе, молочных продуктах, яйцах.
Достаточно белка и в крупах, макаронных изделиях, хлебе, бобовых (сое, чечевице, фасоли, бобах), в орехах и семечках.
Ниже в таблице приведена информация о том, в чем (в каких продуктах питания) содержится белок (азот).
| Продукт | Содержание белка, г/100 г продукта |
| Говядина | 20-22 |
| Свинина | 14-19 |
| Яйца | 12,7 |
| Колбасы, сосиски, сардельки | 9-14 |
| Рыба | 13-23 |
| Молоко и кисломолочные продукты | 2,6-4,3 |
| Творог | 14-18 |
| Сыр | 23-31 |
| Крупы | 7-13 |
| Хлеб | 5-8 |
| Бобовые | 22-23 |
| Овощи | 0,6-4 |
| Картофель | 2 |
| Фрукты | 0,2-2 |
| Орехи | 12-25 |
Еще больше информации о продуктах, богатых белком (азотом) в этом видео:
к оглавлению ↑Допустимо ли сочетать белковые продукты с углеводными
Следующий из системы раздельного питания запрет на совместное употребление белковых и углеводных продуктов теорией рационального питания не обосновывается, да и эволюционно человек приспособлен к потреблению смешанной пищи.
Для полноценного усвоения белка необходимо оптимальное соотношение в нем аминокислот; этому условию отвечает смешанное растительно-животное питание.
Соблюдая рекомендации по разнообразному питанию и нормам потребления белка, удается обеспечить организм достаточным количеством белка и аминокислот без приема пищевых добавок.
к оглавлению ↑Дополнительные рекомендации и советы
Помимо белков, азот включен и в состав азотсодержащих экстрактивных веществ и пуриновых оснований.

Содержащие азот экстрактивные вещества возбуждают железы желудка и способствуют лучшему усвоению белков и жиров в продуктах питания и еде.
Однако эти вещества оказывают и неблагоприятное воздействие на нервную систему, что осложняет течение болезней органов кровообращения, желудочно-кишечного тракта, почек и нервной системы.
Поэтому из диетического питания исключаются первые блюда на мясных и рыбных бульонах, жареные или тушеные вторые блюда.
Пуриновые основания нарушают обменные процессы в организме, что приводит к задержке мочевой кислоты и отложениям ее солей в тканях — основной причине подагры.
Но пуриновые основания являются также обязательным компонентом питания, и их оптимальный уровень в организме поддерживается употреблением хорошо вываренного мяса.
На Земле химический элемент азот присутствует в атмосфере, составляя большую ее часть. Азот входит в состав белков живых организмов, но они не способны усваивать атмосферный азот напрямую.
Азот поступает к ним с белковой пищей или из содержащихся в почве нитратов. В начале цепи превращения атмосферного азота в белки стоят живущие в почве бактерии рода Азотобактер.
Вконтакте
Одноклассники
Мой мир
Узнайте о требованиях к чистоте азота в приложении
Как и большинство обрабатываемых материалов, коммерчески доступный азот не имеет 100% чистоты. Он содержит, по крайней мере, некоторые следовые количества других загрязняющих веществ. Это то же самое, что и при очистке других веществ, например нефтепродуктов. После обработки остаются небольшие следы.
Чем выше степень чистоты, тем выше стоимость. Вот почему так важно найти степень чистоты газообразного азота, соответствующую вашему конкретному применению.
Азот используется в самых разных отраслях промышленности. В качестве инертного газа газообразный азот используется в различных областях - от пищевой промышленности и медицинских испытаний до продувки трубопроводов для сырой нефти. К счастью, азот экономичен и практичен. Часто люди ожидают, что использование азота будет связано с транспортировкой баллонов со сжатым газом на объект.
Фактически, покупка генераторов азота NiGen для производства азота на месте может сделать использование азота чрезвычайно удобным и экономичным.Производство азота на месте также избавляет от необходимости хранить переносные цистерны и планировать доставку цистерн.
Класс чистоты азота
Азот можно производить различной степени чистоты. Чем меньше загрязняющих веществ в азоте, тем выше уровень чистоты и выше затраты на производство азота.
Маркам азота присваиваются разные названия в зависимости от отрасли и производителя азота. Это связано с тем, что для марок азота не существует стандартизированных требований к наименованию.Вместо того, чтобы полагаться на название марки, важно проверить спецификации чистоты азота.
Азот высокой чистоты
В азотной промышленности термин «высокая чистота» обычно означает любой азот, который состоит из более чем 99,9% азота. Азот высокой чистоты часто называют разными названиями в зависимости от производителя.
Из маркетинговых соображений компании часто присваивают азоту высокой чистоты такие названия, как сверхвысокая чистота или исследовательский класс.
Нулевое содержание - еще один общий термин для обозначения азота, который содержит менее 0,5 частей на миллион общего количества углеводородов. Азот высокой чистоты обычно содержит не более 0,5 частей на миллион кислорода и одну часть на миллион диоксида углерода и монооксида углерода. Содержание воды также ограничено до не более трех частей на миллион.
Азот низкой чистоты
Азот с чистотой от 90% до 99,9% имеет низкую чистоту, хотя приведенные названия могут сбивать с толку.Азот низкой чистоты может быть помечен поставщиком как «Высокочистый», поэтому по-прежнему важно проверять конкретные уровни загрязняющих веществ.
В зависимости от области применения, не менее важно учитывать процентное содержание конкретных примесей, таких как кислород или влага, в дополнение к общему уровню чистоты.

Степени чистоты газообразного азота по применению
Необходимый уровень чистоты, количество и типы допустимых загрязнителей зависят от отрасли и области применения.Например, когда возникает проблема сгорания, уровень кислорода может иметь наибольшее значение. Содержание влаги в азоте может стать серьезной проблемой, когда потенциальной проблемой является коррозия.
Технические условия на азот промышленного класса
Азот используется в широком спектре промышленных применений, но для большинства из них требуется только азот низкой чистоты. Азот промышленного сорта обычно должен иметь степень чистоты 95-97%, в зависимости от области применения.
Металлургическая промышленность ценит азот для самых разных целей.Например, азот используется для барботажа расплавленного металла во время дегазации алюминия и для предотвращения образования оксидов во время экструзии алюминия.
При дегазации алюминия расплавленный металл барботируется азотом, выталкивая водород, который может вызвать газовую окклюзию. Для дегазации алюминия требуется чистота не менее 97%.
При экструзии алюминия подходит азот чистотой 99,5% или выше. Это предотвращает образование оксидов на металле.
Такой же или более низкий уровень чистоты подходит для азотной лазерной резки, когда азот используется для ограничения окисления и удаления пыли.Загрязнения в воздухе могут вызвать рассеивание лазерной энергии, что делает азот лучшим вариантом, когда требуется более чистый лазерный разрез.
Нефтяная и газовая промышленность полагаются на инертные свойства азота из соображений безопасности, поскольку присутствие кислорода может привести к проблемам с горючими веществами. Компания по обслуживанию трубопроводов, например, может приобрести портативные генераторы азота NiGen для тестирования трубопроводов и других объектов. Это может включать использование азота для проверки на утечки после ремонта, толкание интеллектуальных трубопроводных скребков или продувку трубопроводов.Портальные генераторы азота могут быть легко перемещены в удаленные места трубопроводов или хранилищ, чтобы азот можно было производить там и тогда, когда это необходимо.
Азот может удалять воздух из резервуаров и трубопроводов для удаления легковоспламеняющегося кислорода, который может представлять угрозу безопасности. Затем азот с низким содержанием влаги продлевает срок службы трубопроводов и защитных резервуаров, устраняя влагу, которая ускоряет развитие ржавчины. Перед вводом в эксплуатацию газовые турбины можно герметизировать подушкой из промышленного азота.В нефтяной промышленности обычно требуется чистота азота в диапазоне 95-99%.
Другие области применения азота промышленного класса включают продувку воздухом из шахт и других закрытых помещений для удаления кислорода и других горючих газов с целью снижения риска пожаров и взрывов. Если вам нужен азот только периодически, вы можете в любое время связаться с NiGen для аренды промышленного генератора азота, чтобы удовлетворить ваши потребности в азоте.
Технические условия на азот для пищевых продуктов
Пищевой азот требует 98% -99.Уровень чистоты 5%. Азот во многих случаях используется в пищевой промышленности в качестве криогенного агента. Продувка воздухом азотом продлевает срок службы упакованных пищевых продуктов за счет уменьшения обесцвечивания и порчи, помогая сохранить аромат. Применение азота в пищевой промышленности включает его использование при розливе вин в бутылки, упаковке сухих пищевых продуктов, таких как кофе, и в производстве продуктов длительного хранения.
Чтобы подавить рост определенных видов бактерий в пище, азот можно смешивать с небольшим количеством кислорода или углекислого газа.Замена кислорода азотом помогает защитить масла в пище от прогорклости, чтобы они дольше оставались свежими. Пищевая упаковка, промываемая азотом, удаляет воздух и загрязняющие вещества, такие как бактерии, которые могут содержаться в воздухе. Пищевой азот обычно содержит низкие уровни окиси углерода и двуокиси углерода и ограниченное количество влаги.
Спецификация газообразного азота медицинского класса
Азот медицинского класса обычно имеет чистоту 99%. Азот используется в газовой форме для наполнения медицинских инструментов и вытеснения воздуха из медицинских сосудов и оборудования.
Жидкий азот используется для криохирургии, которая является распространенным способом удаления кожных образований и некоторых видов рака. Образцы тканей, клеток и крови также можно сохранить с помощью жидкого азота. Быстро застывает, не допуская окисления. Генераторы азота высокой чистоты могут производить необходимый азот на месте, так что он всегда доступен в медицинских и лабораторных помещениях, когда это необходимо.
Технические условия на азот фармацевтического качества
В фармацевтической промышленности используется азот высокой чистоты для различных целей.Азот используется для упаковки лекарств, чтобы удалить кислород и другие загрязнители, которые могут вызвать более быстрое разложение лекарств. Азот может очищать воздух от оборудования и сосудов, чтобы гарантировать, что загрязнение не повлияет на результаты тестирования и не ухудшит качество лекарств в процессе их производства. Азот фармацевтической чистоты имеет уровень чистоты 97% -99,9995%.
Независимо от ваших потребностей в азоте, у NiGen есть азотная система для вас. Свяжитесь с NiGen сегодня. для получения практичных и экономичных азотных растворов, независимо от ваших требований к чистоте азота.
.
азота | Факты, определение, использование, свойства и открытие
Азот (N) , неметаллический элемент 15 группы [Va] периодической таблицы Менделеева. Это бесцветный газ без запаха и вкуса, который является самым распространенным элементом в атмосфере Земли и является составной частью всего живого.
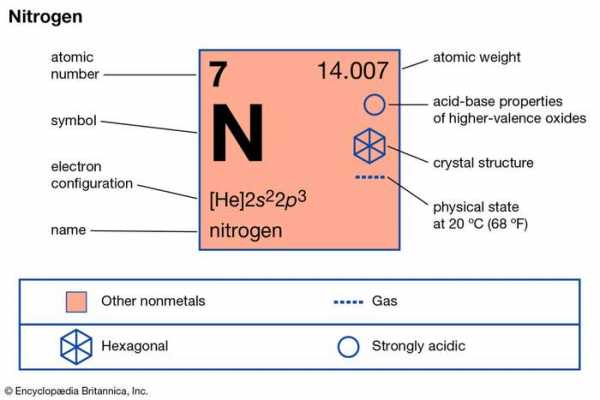 Encyclopædia Britannica, Inc.
Encyclopædia Britannica, Inc. 
Британская викторина
118 Названия и символы из таблицы Менделеева
La
| атомный номер | 7 |
|---|---|
| атомный вес | 14.0067 |
| точка плавления | −209,86 ° C (−345,8 ° F) |
| точка кипения | −195,8 ° C (−320,4 ° F) |
| плотность (1 атм, 0 ° C) | 1,2506 г / л |
| обычные степени окисления | −3, +3, +5 |
| электронная конфигурация | 1 с 2 2 с 2 2 p 3 |
История
Около четырех пятых атмосферы Земли - это азот, который был выделен и признан особенным веществом во время ранних исследований воздуха.Карл Вильгельм Шееле, шведский химик, показал в 1772 году, что воздух представляет собой смесь двух газов, один из которых он назвал «огненным воздухом», потому что он поддерживает горение, а другой «грязным воздухом», потому что он остался после « огненный воздух ». «Огненный воздух» - это, конечно, кислород, а «грязный воздух» - азот. Примерно в то же время азот был признан шотландским ботаником Дэниелом Резерфордом (который первым опубликовал свои открытия), британским химиком Генри Кавендишем и британским священником и ученым Джозефом Пристли, который вместе с Шееле дается заслуга в открытии кислорода.Более поздние работы показали, что новый газ является составной частью селитры, общего названия нитрата калия (KNO 3 ), и, соответственно, французский химик Жан-Антуан-Клод Шапталь в 1790 году назвал его азотом. считался химическим элементом Антуаном-Лораном Лавуазье, чье объяснение роли кислорода в горении в конечном итоге опровергло теорию флогистона, ошибочное представление о горении, которое стало популярным в начале 18 века. Неспособность азота поддерживать жизнь (по-гречески: zoe ) побудила Лавуазье назвать его азот , по-прежнему французский эквивалент азота .
Возникновение и распространение
Среди элементов азот занимает шестое место по количеству в космосе. Атмосфера Земли состоит из 75,51 процента по весу (или 78,09 процента по объему) азота; это основной источник азота для торговли и промышленности. Атмосфера также содержит различные небольшие количества аммиака и солей аммония, а также оксидов азота и азотной кислоты (последние вещества образуются во время грозы и в двигателе внутреннего сгорания).Свободный азот содержится во многих метеоритах; в газах вулканов, шахт и некоторых минеральных источников; на солнце; и в некоторых звездах и туманностях.
Азот также присутствует в минеральных отложениях селитры или селитры (нитрат калия, KNO 3 ) и чилийской селитры (нитрат натрия, NaNO 3 ), но эти отложения существуют в количествах, которые совершенно не соответствуют потребностям человека. Еще один богатый азотом материал - гуано, которое можно найти в пещерах летучих мышей и в сухих местах, часто посещаемых птицами.В сочетании азот содержится в дожде и почве в виде аммиака и солей аммония, а в морской воде - в виде аммония (NH 4 + ), нитрита (NO 2 - ) и нитрата (NO 3 ). - ) ионы. Азот составляет в среднем около 16 процентов по массе сложных органических соединений, известных как белки, присутствующих во всех живых организмах. Естественное содержание азота в земной коре составляет 0,3 части на 1000 человек. Космическое содержание - предполагаемое общее содержание во Вселенной - составляет от трех до семи атомов на атом кремния, что считается стандартом.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняИндия, Россия, США, Тринидад и Тобаго и Украина входили в пятерку крупнейших производителей азота (в форме аммиака) в начале 21 века.
Коммерческое производство и использование
Промышленное производство азота в основном осуществляется путем фракционной перегонки сжиженного воздуха. Температура кипения азота составляет -195,8 ° C (-320,4 ° F), что примерно на 13 ° C (-23 ° F) ниже, чем у кислорода, который поэтому остается позади.Азот также можно производить в больших масштабах путем сжигания углерода или углеводородов в воздухе и отделения образующихся диоксида углерода и воды от остаточного азота. В небольших масштабах чистый азот получают путем нагревания азида бария, Ba (N 3 ) 2 . Различные лабораторные реакции, в результате которых образуется азот, включают нагревание растворов нитрита аммония (NH 4 NO 2 ), окисление аммиака бромной водой и окисление аммиака горячим оксидом меди.
Элементарный азот можно использовать в качестве инертной атмосферы для реакций, требующих исключения кислорода и влаги.В жидком состоянии азот имеет ценные криогенные применения; за исключением газов водорода, метана, окиси углерода, фтора и кислорода, практически все химические вещества имеют пренебрежимо малое давление пара при температуре кипения азота и поэтому существуют в виде кристаллических твердых веществ при этой температуре.
В химической промышленности азот используется для предотвращения окисления или другого порчи продукта, в качестве инертного разбавителя реактивного газа, в качестве носителя для отвода тепла или химикатов, а также в качестве ингибитора пожара или взрывов.В пищевой промышленности газообразный азот используется для предотвращения порчи из-за окисления, плесени или насекомых, а жидкий азот используется для сублимационной сушки и для холодильных систем. В электротехнической промышленности азот используется для предотвращения окисления и других химических реакций, для создания избыточного давления в оболочках кабелей и для защиты двигателей. Азот находит применение в металлургической промышленности при сварке, пайке и пайке, где он помогает предотвратить окисление, науглероживание и обезуглероживание. В качестве инертного газа азот используется для производства вспененного или вспененного каучука, пластиков и эластомеров, в качестве газа-вытеснителя для аэрозольных баллончиков и для повышения давления жидких пропеллентов для реакционных струй.В медицине быстрое замораживание жидким азотом может использоваться для сохранения крови, костного мозга, тканей, бактерий и спермы. Жидкий азот также оказался полезным в криогенных исследованиях.
.фактов об азоте | Живая наука
Азот необходим для жизни на Земле. Это компонент всех белков, и его можно найти во всех живых системах. Соединения азота присутствуют в органических материалах, продуктах питания, удобрениях, взрывчатых веществах и ядах. Азот имеет решающее значение для жизни, но его избыток также может быть вредным для окружающей среды.
Названный в честь греческого слова nitron , обозначающего «природная сода», и генов , обозначающего «формирование», азот является пятым по распространенности элементом во Вселенной.По данным Лос-Аламосской национальной лаборатории, газообразный азот составляет 78 процентов воздуха Земли. С другой стороны, атмосфера Марса состоит всего на 2,6 процента азота.
В газообразной форме азот не имеет цвета, запаха и обычно считается инертным. По словам Лос-Аламоса, в жидкой форме азот также не имеет цвета и запаха и похож на воду.
Только факты
- Атомный номер (число протонов в ядре): 7
- Атомный символ (в Периодической таблице элементов): N
- Атомный вес (средняя масса атома): 14.0067
- Плотность: 0,0012506 грамм на кубический сантиметр
- Фаза при комнатной температуре: газ
- Точка плавления: минус 321 градус по Фаренгейту (минус 210 градусов Цельсия)
- Точка кипения: минус 320,42 F (минус 195,79 C)
- Количество изотопов (атомов одного элемента с разным числом нейтронов): 16, включая 2 стабильных
- Наиболее распространенные изотопы: Азот-14 (Изобилие: 99,63 процента)
Азот (Изображение предоставлено: general-fmv, Андрей Маринкас Shutterstock)
Компонент удобрения
Азот был открыт в 1772 году химиком и врачом Дэниелом Резерфордом, когда он удалил кислород и углекислый газ из воздуха, продемонстрировав, что остаточный газ не поддерживает живые организмы или горение, по данным Лос-Аламосской национальной лаборатории.Другие ученые, в том числе Карл Вильгельм Шееле и Джозеф Пристли, работали над той же проблемой и называли азот «обожженным» воздухом или воздухом без кислорода. В 1786 году Антуан Лоран де Лавуазье назвал азот азотом, что означает «безжизненный». Это было основано на наблюдении, что часть воздуха не может поддерживать жизнь сама по себе.
Одним из наиболее важных соединений азота является аммиак (NH 3 ), который может быть произведен в так называемом процессе Габера-Боша, в котором азот реагирует с водородом.Бесцветный газообразный аммиак с резким запахом можно легко превратить в азотное удобрение. Фактически, около 80 процентов производимого аммиака используется в качестве удобрений. Он также используется в качестве хладагента; в производстве пластмасс, текстиля, пестицидов и красителей; и в чистящих растворах, по данным Государственного департамента Нью-Йорка.
Азотный цикл
Азотный цикл, в котором атмосферный азот превращается в различные органические соединения, является одним из наиболее важных естественных процессов для поддержания жизни живых организмов.Во время цикла бактерии в почве обрабатывают или «фиксируют» атмосферный азот в аммиак, который необходим растениям для роста. Другие бактерии превращают аммиак в аминокислоты и белки. Затем животные едят растения и потребляют белок. Соединения азота возвращаются в почву с отходами животноводства. Бактерии превращают отработанный азот обратно в газообразный азот, который возвращается в атмосферу.
Стремясь ускорить рост сельскохозяйственных культур, люди используют азот в удобрениях. Однако чрезмерное использование этих удобрений в сельском хозяйстве имело разрушительные последствия для окружающей среды и здоровья человека, поскольку оно способствовало загрязнению грунтовых и поверхностных вод.По данным Агентства по охране окружающей среды США (EPA), загрязнение питательными веществами, вызванное избытком азота и фосфора в воздухе и воде, является одной из наиболее распространенных, дорогостоящих и сложных экологических проблем.
Устранение дисбаланса
Одно из решений проблемы избыточного азота заключается в устойчивом сельском хозяйстве, органическом земледелии и повышении осведомленности фермеров об этих экологических проблемах, по словам Рэнди А. Дальгрена, профессора почвоведения Университета Калифорния, Дэвис.
«Идея состоит в том, чтобы попытаться отказаться от использования этих коммерческих удобрений и вместо этого использовать органические отходы», например, отходы животноводства, - сказал он. Другим шагом было бы использование удобрений с медленным высвобождением, которые имеют пластиковое покрытие, и вместо того, чтобы сразу выделять азот, высвобождение азота происходит постепенно в течение всего вегетационного периода, «пытаясь сопоставить выделение азота из удобрений с пластиковым покрытием с потребности завода ", - сказал он.
Микробиологи из Университета Альберты в Канаде и Венского университета в Австрии, возможно, обнаружили другое решение.В августе 2017 года исследователи объявили, что идентифицировали микроб, окисляющий аммиак, под названием Nitrospira inopinata .
По словам исследователей, Nitrospira inopinata - это аммиачная губка, которая существенно превосходит почти все другие типы бактерий и архей (одноклеточные организмы) в окислении аммония в окружающей среде. Поскольку этот микроб является таким эффективным окислителем, он может производить меньше закиси азота в процессе.
Новые открытия, опубликованные в научном журнале Nature, могут иметь важное значение для исследований изменения климата.Исследователи готовы испытать этот микроб с помощью различных практических приложений, которые могут снизить уровень аммония в почве, воде и атмосфере. По данным Университета Альберты, некоторые из этих приложений могут включать изменения в нашей питьевой воде, очистке сточных вод и очистке почвы.
Кто знал?
- Несмотря на то, что термин «азот» используется в английском языке для обозначения этого элемента, термин «азот» Лавуазье все еще используется во французском языке, и его форма присутствует в «азото» на итальянском языке или «азот» на польском языке.
- По данным Королевского химического общества, жидкий азот часто используется в качестве хладагента, например, для хранения спермы, яиц и других клеток, используемых в медицинских исследованиях или клиниках репродуктивной медицины.
- Жидкий азот также используется для быстрой заморозки продуктов и помогает сохранить их вкус, текстуру, влажность и аромат.
- Азот составляет 95 процентов атмосферы Титана (крупнейшего спутника Сатурна), по данным Лаборатории реактивного движения.
- Газообразный азот играет роль в формировании полярного сияния - естественного проявления света в небе, которое можно преимущественно наблюдать в арктических и антарктических регионах, - которое возникает, когда быстро движущиеся электроны из космоса сталкиваются с кислородом и азотом в нашей атмосфере. по данным НАСА.
- Газообразный азот можно получить путем нагревания водного раствора нитрата аммония (Nh5NO3), твердого кристаллического вещества, которое обычно используется в удобрениях.
- По данным Королевского химического общества, с использованием процесса Габера ежегодно производится около 150 тонн аммиака.
- По данным Королевского химического общества, азот в форме хлорида аммония, Nh5Cl, производился в Древнем Египте путем нагревания смеси экскрементов животных, мочи и соли.
- Нитроглицерин, сильнодействующее взрывчатое вещество, используемое при производстве динамита, представляет собой маслянистую бесцветную жидкость, содержащую азот, кислород и углерод.
Дополнительный отчет от Трейси Педерсен, сотрудника Live Science.
Дополнительные ресурсы
- На этом веб-сайте описывается, что происходит, когда вы пытаетесь поместить различные предметы в жидкий азот.
- Эта инфографика иллюстрирует загрязнение азотом Чесапикского залива.
Онлайн-анализ азотсодержащих соединений в сложных углеводородных матрицах
Хроматограмма, полученная с использованием автономной ГХХГХ-НКД для определения характеристик азотсодержащих соединений в образце сланцевого масла, приведена на рис. 3 . Выделены следующие классы: пиридины, анилины, хинолины, индолы, акридины и карбазолы. Кроме того, была возможна подробная количественная оценка отдельных соединений. Собранные данные были использованы для определения индивидуальных концентраций соединений, и полученные значения представлены в Таблице 5 .Анализируемый образец содержит 4,21 мас.% Азотсодержащих соединений, в основном принадлежащих к классу пиридинов. С точки зрения обработки такое высокое содержание азота вызывает беспокойство, когда считается, что сланцевое масло заменяет традиционное сырье для парового крекинга, где азотсодержащие соединения обычно присутствуют только в количествах ppm.
Оперативный анализ выходящего потока реактора во время пиролиза смеси пиридин-гептан при температуре на выходе змеевика (COT) 1073 K и давлении на выходе змеевика (COP) 170 кПа, выполненный с помощью GC × GC-TOF-MS ( см. , рис. 4a. ), использовался для идентификации продуктов реакции и установления времени удерживания соединения для конкретного набора рабочих условий ГХ × ГХ.Анализ ГХ × ГХ – ПИД (см. , рис. 4b, ) использовался для определения состава выходящего потока реактора при использовании пара в качестве разбавителя. Полученные концентрации продукта, приведенные к 100%, приведены в Таблице 6 . Идентифицированные продукты на этих хроматограммах показывают, что реакции присоединения пиридина благоприятны по сравнению с разложением пиридина. Хаузер и Лифшиц 29,30 сообщили об образовании легких нитрилов в экспериментах по пиролизу пиридина и пиррола.Поскольку эти молекулы не были обнаружены в данной серии экспериментов, а молярные балансы азота в экспериментах закрыты, можно сделать вывод, что пиридин не разлагается в значительной степени при выбранных условиях процесса.
Тестирование онлайн-метода GC × GC – NCD было проведено в отдельном эксперименте в условиях, исключающих разложение пиридина, , т.е. , температуре 823 K и COP 170 кПа. К потоку азота и воды добавляли пиридин с концентрацией 841,4 м.д. по массе, и после добавления внутреннего стандарта пробу выходящего из реактора потока вводили на ГХ × ГХ.Используя полученный отклик детектора и известную концентрацию внутреннего стандарта, была измерена концентрация пиридина 819 ppmw. Следовательно, относительная погрешность измерения была определена как менее 3% (см. Рисунок 5 ).
Наконец, был проведен эксперимент по паровому крекингу гептана в более жестких условиях с небольшим количеством пиридина, добавленным к исходному н-гептану. Эксперимент проводился в типичных условиях парового крекинга с разбавлением водяным паром 0.5 кг / кг, COT 1,123 K и COP 170 кПа. На рис. 6 показаны полученные хроматограммы GC × GC – NCD и FID. Соединения были идентифицированы на основании времени удерживания и данных, полученных с помощью TOF-MS. На хроматограмме GC × GC – NCD были обнаружены следующие соединения: ацетонитрил, пиридин, 2-метилпиридин, 3-метилпиридин, 3-этилпиридин, 3-этенилпиридин, 3-метилбензонитрил, индол. Используя соответствующие индексы удерживания Коваца, можно было предварительно определить 2-бутеннитрил и пропанонитрил.Количественные результаты представлены в Таблице 7 . Массовый расход пиридина в реактор был установлен на 1,2 мг / с, , т.е. , концентрация элементарного азота в реакционной смеси составляла 125,9 частей на миллион по массе. После повторной обработки полученных данных концентрация азота в выходящем из реакции потоке была определена как 124,5 частей на миллион по массе, что соответствует извлечению азота 98,5%.
Рисунок 1. Подробное схематическое изображение печи для отбора проб ГХ × ГХ и клапанов. Клапан 1a показан в положении продувки, промывая контур для отбора проб сточными водами. Клапан 1b показан в положении впрыска: газ-носитель (гелий) перенаправляется в печь для отбора проб, где он используется для транспортировки вытекающей пробы в соответствующий ГХ по транспортной линии 18 . Щелкните здесь, чтобы просмотреть увеличенную версию этого рисунка.
Рисунок 2. Схематическое изображение метода количественного анализа сточных вод в реальном времени с использованием эталонного соединения. Известное количество азота, добавляемого к выходящему потоку, определяется с помощью RGA / TCD и используется для определения концентрации метана, который является эталонным соединением для анализа выходящего потока реактора. Точно так же известное количество 2-хлорпиридина добавляется к выходящему потоку и используется в качестве внутреннего стандарта для анализа GC × GC – NCD. Щелкните здесь, чтобы просмотреть увеличенную версию этого рисунка.
Рис. 3. Хроматограмма GC × GC – NCD пробы сланцевого масла. Внутренний стандарт и разделенные типы азотсодержащих углеводородных групп, пиридинов, анилинов, хинолинов, индолов, акридинов и карбазолов.Щелкните здесь, чтобы просмотреть увеличенную версию этого рисунка.
Рис. 4. Анализ продуктов пиролиза смеси пиридин-гептан. ( a ) GC × GC - TOF-MS хроматограмма, ( b ) GC × GC – FID хроматограмма. Азотсодержащие продукты эксперимента пиролиза, проведенного при COT 1073 K и COP 170 кПа, обозначены заглавными буквами (A: пиридин, B: 2-метилпиридин, C: 3-метилпиридин, D: 4-этилпиридин, E : 3-этенилпиридин, F: 4-этенилпиридин, G: 2-метилбензонитрил, H: хинолин, K: изохинолин, I: 1-H-индол-7-метил, J: индол, L: бензонитрил, M: 4-метилхинолин , N: 5-этенил-2-метилпиридин, O: 7-метилиндолизин).Щелкните здесь, чтобы просмотреть увеличенную версию этого рисунка.
Рис. 5. ГХ × ГХ – НКД обнаружение пиридина в потоке, выходящем из реактора, в режиме реального времени в условиях отсутствия реакции. Эксперимент проводят изотермически при 773 K и COP 170 кПа и используют для оценки метода количественного определения внутреннего стандарта. Щелкните здесь, чтобы просмотреть увеличенную версию этого рисунка.
Рис. 6. Анализ продуктов парового крекинга гептана со следами пиридина. ( a ) Хроматограмма GC × GC – FID ( b ) GC × GC – NCD хроматограмма. Обнаружение основных продуктов парового крекинга с ПИД и незначительных азотсодержащих продуктов парового крекинга с НКД. Эксперимент проводится с разбавлением паром 0,5 кг / кг, COT 1,123 K и COP 170 кПа. Щелкните здесь, чтобы просмотреть увеличенную версию этого рисунка.
| Детектор | NCD |
| Инжектор | 573 К |
| Разделенный поток | 200 мл / мин |
| Газ-носитель | 2.1 мл / мин |
| Начальная температура печи | 313 К |
| Скорость нагрева | 3 К / мин |
| Конечная температура | 573 К |
| Время модуляции | 7 секунд |
| Настройки детектора | |
| Температура | 1,198 К |
| Диапазон | 1 |
| Скорость сбора данных | 100 Гц |
Таблица 1. Обзор условий ГХ × ГХ, применяемых для определения характеристик сланцевой нефти в автономном режиме.
| Детектор | Пиролиз | Паровой крекинг | Метод испытания | Паровой крекинг |
| Расход гептана, г / час | 2,480 | 2 880 | 98,89 | 4 000 |
| Расход воды, г / час | / | 1,440 | 2 000 | 2 000 |
| Расход азота, г / час | / | / | 4 000 | / |
| Расход гелия, г / час | 507 | / | / | / |
| Расход пиридина, г / час | 25.1 | 29,1 | 5,21 | 4,33 |
| Расход 2-хлорпиридина, г / час | / | / | 4,21 | 0,85 |
| Расход гексана, г / час | / | / | 85,91 | 83,63 |
| Температура на выходе змеевика (COT), К | 1 073 | 1 073 | 823 | 1,123 |
| Давление на выходе змеевика (COP), бар | 1.7 | 1,7 | 1,7 | 1,7 |
| Детектор | TOF-MS | FID | NCD | NCD |
Таблица 2. Прикладные экспериментальные условия.
| RGA | |||
| Канал | Канал 1 | Канал 2 | Канал 3 |
| Впрыск | 50 мкл (газ), 353 К | 150 мкл (газ), 353 К | 150 мкл (газ), 353 К |
| Газ-носитель | He | He | № 2 |
| Перед колонкой | Капиллярная предколонка из плавленого кремнезема (15 м × 0.53 мм × 3 мкм) | Колонка с насадочными пористыми полимерами (0,25 м × 3,175 мм) | Колонка с насадочными пористыми полимерами (1 м × 3,175 мм) |
| Аналитический | Колонка на глиноземной связке (25 м × 0,53 мм × 15 м) | Колонка с насадочными пористыми полимерами (1 м × 3,175 мм, 1 м × 3,175 мм) | Колонка с углеродным молекулярным ситом (2 м × 3,175 мм) |
| Духовка | 323 → 393 К (5 К / мин) | 353 К | 353 К |
| Детектор | FID, 473 К | TCD, 433 К | TCD, 433 К |
Таблица 3.Раздел on-line анализа опытной установки - Настройки RGA.
| Детектор | FID | TOF-MS | NCD |
| Форсунка | 573 К | 573 К | 573 К |
| Разделенный поток | 30 мл / мин | 30 мл / мин | 10 мл / мин |
| Газ-носитель | 2.1 мл / мин | 2,6 мл / мин | 2,1 мл / мин |
| Начальная температура печи | 233 К | 233 К | 233 К |
| Изменение скорости нагрева I | 4 К / мин | 4 К / мин | 4 К / мин |
| Поддержание температуры, не менее | 4 | 4 | 4 |
| Изменение температуры | 313 К | 313 К | 313 К |
| Изменение скорости нагрева II | 5 К / мин | 5 К / мин | 5 К / мин |
| Конечная температура | 573 К | 573 К | 573 К |
| Время модуляции | 5 секунд | 5 секунд | 5 секунд |
| Детектор | |||
| Температура | 573 К | 473 К | 1,198 К |
| Диапазон | 10 | п.а. | 1 |
| Скорость сбора данных | 100 Гц | 30 Гц | 100 Гц |
Таблица 4. Секция оперативного анализа пилотной установки - настройки ГХ × ГХ.
| Углеродный номер | пиридины, мас.% | Анилины, мас.% | хинолинов, мас.% | индолов, мас.% | акридинов, мас.% | карбазолов, мас.% |
| 5 | 0,01 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 6 | 0,04 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 7 | 0.11 | 0,02 | 0,00 | 0,00 | 0,00 | 0,00 |
| 8 | 0,26 | 0,05 | 0,00 | 0,01 | 0,00 | 0,00 |
| 9 | 0,47 | 0,07 | 0,01 | 0,06 | 0,00 | 0,00 |
| 10 | 0.15 | 0,11 | 0,08 | 0,17 | 0,00 | 0,00 |
| 11 | 0,18 | 0,11 | 0,17 | 0,28 | 0,00 | 0,00 |
| 12 | 0,12 | 0,08 | 0,19 | 0,30 | 0,00 | 0,00 |
| 13 | 0.18 | 0,03 | 0,12 | 0,16 | 0,00 | 0,02 |
| 14 | 0,17 | 0,00 | 0,03 | 0,14 | 0,01 | 0,02 |
| 15 | 0,13 | 0,00 | 0,00 | 0,00 | 0,02 | 0,00 |
| 16 | 0.10 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 17 | 0,05 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 18 | 0,03 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 19 | 0.00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 20 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 21 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 22 | 0.00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 23 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 24 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 25 | 0.00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 26 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 27 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 28 | 0.00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 29 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 30 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 31 | 0.00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 32 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 33 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| Всего, мас.% | 1,98 | 0,46 | 0,59 | 1,10 | 0,04 | 0,04 |
Таблица 5. Концентрация азотсодержащих соединений в сланцевом масле.
Таблица 6. Концентрации соединений в выходящем из реактора потоке при крекинге гептана с 1,0 мас.% Пиридина (разбавление паром 0.5 кг / кг, COT 1073 K, COP 170 кПа). Щелкните здесь, чтобы загрузить этот файл.
Таблица 7. Концентрации соединения в выходящем из реактора потоке при паровом крекинге гептана со следами пиридина (разбавление паром 0,5 кг / кг, COT 1,123 K, COP 170 кПа). Щелкните здесь, чтобы загрузить этот файл.
Требуется подписка. Пожалуйста, порекомендуйте JoVE своему библиотекарю.
.