Какие продукты получаются при окислении метилового спирта
Химические свойства спиртов | CHEMEGE.RU
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
Строение, изомерия и гомологический ряд спиртов
Химические свойства спиртов
Способы получения спиртов
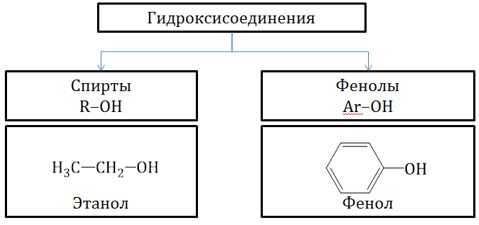
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н+ соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
Таким образом, для спиртов характерны следующие свойства:
|
1. Кислотные свойства
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому спирты не взаимодействуют с растворами щелочей.
Многоатомные спирты также не реагируют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Спирты взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
| Например, этанол взаимодействует с калием с образованием этилата калия и водорода. |
Видеоопыт взаимодействия спиртов (метанола, этанола и бутанола) с натрием можно посмотреть здесь.
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, этилат калия разлагается водой: |
| Кислотные свойства одноатомных спиртов уменьшаются в ряду: CH3OH > первичные спирты > вторичные спирты > третичные спирты |
Многоатомные спирты также реагируют с активными металлами:
Видеоопыт взаимодействия глицерина с натрием можно посмотреть здесь.
1.3. Взаимодействие с гидроксидом меди (II)
Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли (качественная реакция на многоатомные спирты).
| Например, при взаимодействии этиленгликоля со свежеосажденным гидроксидом меди (II) образуется ярко-синий раствор гликолята меди: |
Видеоопыт взаимодействия этиленгликоля с гидроксидом меди (II) можно посмотреть здесь.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, этанол реагирует с бромоводородом. |
Видеоопыт взаимодействия этилового спирта с бромоводородом можно посмотреть здесь.
| Реакционная способность одноатомных спиртов в реакциях с галогеноводородами уменьшается в ряду: третичные > вторичные > первичные > CH3OH. |
Многоатомные спирты также, как и одноатомные спирты, реагируют с галогеноводородами.
| Например, этиленгликоль реагирует с бромоводородом: |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии этанола с аммиаком образуется этиламин. |
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты): |
Многоатомные спирты вступают в реакции этерификации с органическими и неорганическими кислотами.
| Например, этиленгликоль реагирует с уксусной кислотой с образованием ацетата этиленгликоля: |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат: |
| Например, глицерин под действием азотной кислоты образует тринитрат глицерина (тринитроглицерин): |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре (больше 140оС) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
| Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен: |
В качестве катализатора этой реакции также используют оксид алюминия.
| Отщепление воды от несимметричных спиртов проходит в соответствии с правилом Зайцева: водород отщепляется от менее гидрогенизированного атома углерода. |
| Например, в присутствии концентрированной серной кислоты при нагревании выше 140оС из бутанола-2 в основном образуется бутен-2: |
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140оС) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации этанола при температуре до 140оС образуется диэтиловый эфир: |
4. Окисление спиртов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
| При окислении первичных спиртов они последовательно превращаются сначала в альдегиды, а потом в карбоновые кислоты. Глубина окисления зависит от окислителя. Первичный спирт → альдегид → карбоновая кислота |
| Метанол окисляется сначала в формальдегид, затем в углекислый газ: Метанол → формальдегид → углекислый газ |
| Вторичные спирты окисляются в кетоны: вторичные спирты → кетоны |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
Легкость окисления спиртов уменьшается в ряду:
метанол < первичные спирты < вторичные спирты < третичные спирты
Продукты окисления многоатомных спиртов зависят от их строения. При окислении оксидом меди многоатомные спирты образуют карбонильные соединения.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
| Например, этанол окисляется оксидом меди до уксусного альдегида |
Видеоопыт окисления этанола оксидом меди (II) можно посмотреть здесь.
| Например, пропанол-2 окисляется оксидом меди (II) при нагревании до ацетона |
Третичные спирты окисляются только в жестких условиях.
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
| Например, при окислении пропанола-1 образуется пропаналь |
Видеоопыт каталитического окисления этанола кислородом можно посмотреть здесь.
| Например, пропанол-2 окисляется кислородом при нагревании в присутствии меди до ацетона |
Третичные спирты окисляются только в жестких условиях.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот, вторичные спирты окисляются до кетонов, метанол окисляется до углекислого газа.
| При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси. |
Третичные спирты окисляются только в жестких условиях (в кислой среде при высокой температуре) под действием сильных окислителей: перманганатов или дихроматов. При этом происходит разрыв углеродной цепи и могут образоваться углекислый газ, карбоновая кислота или кетон, в зависимости от строения спирта.
| Спирт/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метанол СН3-ОН | CO2 | K2CO3 |
| Первичный спирт R-СН2-ОН | R-COOH/ R-CHO | R-COOK/ R-CHO |
| Вторичный спирт R1-СНОН-R2 | R1-СО-R2 | R1-СО-R2 |
| Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ |
| Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота |
| Например, при взаимодействии изопропанола с перманганатом калия в серной кислоте образуется ацетон |
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
CnH2n+1ОН + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
| Например, уравнение сгорания метанола: |
2CH3OH + 3O2 = 2CO2 + 4H2O
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола и первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов образуются кетоны.
| Например, при дегидрировании этанола образуется этаналь |
| Например, при дегидрировании этиленгликоля образуется диальдегид (глиоксаль) |
алкоголя | Определение, формула и факты
Спирт , любой из класса органических соединений, характеризующихся одной или несколькими гидроксильными (OH) группами, присоединенными к атому углерода алкильной группы (углеводородной цепи). Спирты можно рассматривать как органические производные воды (H 2 O), в которых один из атомов водорода замещен алкильной группой, обычно представленной R в органических структурах. Например, в этаноле (или этиловом спирте) алкильная группа представляет собой этильную группу, ―CH 2 CH 3 .
Спирты относятся к наиболее распространенным органическим соединениям. Они используются в качестве подсластителей и при создании духов, являются ценными промежуточными продуктами в синтезе других соединений и являются одними из наиболее широко производимых органических химикатов в промышленности. Возможно, два самых известных спирта - этанол и метанол (или метиловый спирт). Этанол используется в туалетных принадлежностях, фармацевтических препаратах и топливе, а также для стерилизации больничных инструментов. Кроме того, это алкоголь в спиртных напитках.Анестезирующий эфир также производится из этанола. Метанол используется как растворитель, как сырье для производства формальдегида и специальных смол, в специальных топливах, в антифризах и для очистки металлов.
Спирты можно разделить на первичные, вторичные или третичные, в зависимости от того, какой углерод алкильной группы связан с гидроксильной группой. Большинство спиртов представляют собой бесцветные жидкости или твердые вещества при комнатной температуре. Спирты с низким молекулярным весом хорошо растворяются в воде; с увеличением молекулярной массы они становятся менее растворимыми в воде, и их температура кипения, давление пара, плотность и вязкость повышаются.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняВ этой статье рассматриваются структура и классификация, физические свойства, коммерческое значение, источники и реакции спиртов. Для получения дополнительной информации о тесно связанных соединениях, см. химическое соединение, фенол и эфир.
.алкоголя | Определение, формула и факты
Спирт , любой из класса органических соединений, характеризующихся одной или несколькими гидроксильными (OH) группами, присоединенными к атому углерода алкильной группы (углеводородной цепи). Спирты можно рассматривать как органические производные воды (H 2 O), в которых один из атомов водорода замещен алкильной группой, обычно представленной R в органических структурах. Например, в этаноле (или этиловом спирте) алкильная группа представляет собой этильную группу, ―CH 2 CH 3 .
Спирты относятся к наиболее распространенным органическим соединениям. Они используются в качестве подсластителей и при создании духов, являются ценными промежуточными продуктами в синтезе других соединений и являются одними из наиболее широко производимых органических химикатов в промышленности. Возможно, два самых известных спирта - этанол и метанол (или метиловый спирт). Этанол используется в туалетных принадлежностях, фармацевтических препаратах и топливе, а также для стерилизации больничных инструментов. Кроме того, это алкоголь в спиртных напитках.Анестезирующий эфир также производится из этанола. Метанол используется как растворитель, как сырье для производства формальдегида и специальных смол, в специальных топливах, в антифризах и для очистки металлов.
Спирты можно разделить на первичные, вторичные или третичные, в зависимости от того, какой углерод алкильной группы связан с гидроксильной группой. Большинство спиртов представляют собой бесцветные жидкости или твердые вещества при комнатной температуре. Спирты с низким молекулярным весом хорошо растворяются в воде; с увеличением молекулярной массы они становятся менее растворимыми в воде, и их температура кипения, давление пара, плотность и вязкость повышаются.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняВ этой статье рассматриваются структура и классификация, физические свойства, коммерческое значение, источники и реакции спиртов. Для получения дополнительной информации о тесно связанных соединениях, см. химическое соединение, фенол и эфир.
.Реакция трийодметана (йодоформа) со спиртами
Использование раствора йода и гидроксида натрия
Это химически более очевидный метод.
Раствор йода добавляют к небольшому количеству спирта, а затем добавляют столько раствора гидроксида натрия, чтобы обесцветить йод. Если на морозе ничего не происходит, возможно, придется очень осторожно подогреть смесь.
Положительный результат - появление очень бледно-желтого осадка трийодметана (ранее известного как йодоформ) - CHI 3 .
Помимо цвета, это можно узнать по слабому «лечебному» запаху. Его используют как антисептик, например, на липких пластырях, которые наносят на небольшие порезы.
Использование растворов йодида калия и хлората натрия (I)
Хлорат натрия (I) также известен как гипохлорит натрия.
К небольшому количеству спирта добавляют раствор йодида калия, а затем раствор хлората натрия (I). Опять же, если на холоде не образуется осадка, возможно, придется очень осторожно нагреть смесь.
Положительный результат - такой же бледно-желтый осадок, что и раньше.
.Руководство для промышленности: Временная политика по приготовлению определенных дезинфицирующих средств для рук на спиртовой основе во время чрезвычайной ситуации в области общественного здравоохранения (COVID-19)
- Номер дела:
- FDA-2020-D-1106
- Выдал:
-
Отдел выдачи руководств
Центр оценки и исследований лекарственных средств
Обновлено 1 июня 2020 г.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA или Агентство) играет критически важную роль в защите Соединенных Штатов от новых инфекционных заболеваний, таких как пандемия коронавирусной болезни 2019 (COVID-19).FDA стремится предоставлять своевременные рекомендации для поддержки непрерывности и усилий по реагированию на эту пандемию.
Добавить комментарии
Вы можете отправить онлайн или письменные комментарии по любому руководству в любое время (см. 21 CFR 10.115 (g) (5))
Если вы не можете отправить комментарии в режиме онлайн, отправьте письменные комментарии по адресу:
Управление картотеки
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов
5630 Fishers Lane, Rm 1061
Rockville, MD 20852
Все письменные комментарии должны быть обозначены номером в реестре этого документа: FDA-2020-D-1106.
-
Текущее содержание с:
-
Регулируемые продукты
Тема (и)
Тема (и) здравоохранения










