Иммунодефициты первичные и вторичные
Первичные и вторичные иммунодефициты

Иммунодефицитное состояние — это патология, которая связана со снижением функциональной активности одного или нескольких основных компонентов иммунитета. В результате чего происходит нарушение защиты организма от микробов, приводящее к повышенной инфекционной заболеваемости. Иммунодефициты являются предрасполагающим фактором для развития инфекций, аутоиммуных нарушений, лимфом и прочих болезней. Нередко эта проблема протекает бессимптомно, маскируясь под обычные сезонные простуды. Как правило, диагностирование происходит после нескольких перенесенных болезней, которые возникают слишком часто и беспочвенно. В современной практике выделяют 2 вида иммунодефицитных состояний: первичный и вторичный . Каждый из которых имеет свои отличительные особенности.
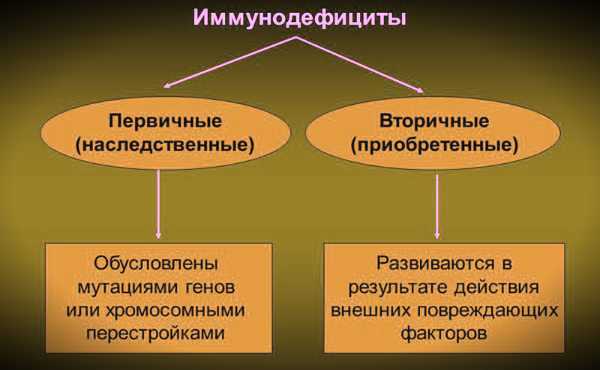
Первичные иммунодефициты
Они генетически детерминированы, могут проявляться в качестве отдельных синдромов или быть их составляющей. Сегодня описано больше 100 подобных патологии, в пределах которых может выявляться определенная гетерогенность. В большинстве случаев, первичный иммунодефицит начинает проявляться в раннем детстве (младенчество или дошкольный возраст) в виде частных и нестандартных инфекционных процессов. Согласно статистике, яркая клиническая картина возникает у больных до 20 лет. Одной из главных проблем, с которыми сталкиваются врачи при встрече с данным диагнозом, является разная симптоматика. В связи с тем, что при первичном иммунодефиците могут поражаться несколько звеньев иммунитета, клиническая картина может иметь разнообразный характер у каждого больного.
Причины и виды первичных иммунодефицитов
Основным этиологическим факторам этой патологии служит генетический сбой в иммунной системе. В результате чего происходит недостаточное формирование защитных механизмов в организме ребенка. Это приводит к тому, что больной не может противостоять инфекциям, регулярно заболевает различными болезнями. В медицинской практике активно используется классификация первичного иммунодефицита, включающая в себя 5 групп, которые отличаются в зависимости от пораженного звена. Это:
- Гуморальный — связан с нарушением образования антител. Является наиболее распространенным видом. На долю которого приходится порядка 50-60%.
- Клеточный — вызван нарушением дифференцировки и деления лимфоцитов. На его долю приходится не более 10%.
- Комбинированный — гуморальный и клеточный иммунодефицит. Занимает второе место по распространенности, охватывая около 20% больных.
- Иммунодефицит, вызванный недостаточностью фагоцитов. Составляет от 10 до 15% случаев. Нарушает способность фагоцитарный клеток уничтожать патогенные микроорганизмы. Для этой разновидности больше всего характерно появление кожных инфекций, вызванных стафилококками и грамотрицательной микрофлорой.
- Комплементарный. Встречается достаточно редко (составляет менее 2%). Включает в себя отдельные расстройства компонентов комплемента. Может иметь как наследственный (бывают аутосомными и рецессивными), так и приобретенный характер. Такие состояния приводят к дефективным опсонизациям, фагоцитозу и лизису патогенетических объектов, равно как и к недостаточной чистке комплексов АГ-АТ. Наиболее серьезными и жизнеугрожающими представителями данной категории служит СКВ и аутоиммунный гломерулонефрит.
Симптомы первичного иммунодефицита
Как указывалось выше, первичный иммунодефицит начинает проявляться в детском возрасте. Наиболее существенной проблемой этого состояния служит высокая восприимчивость больного организма к инфекционным процессам. Люди с этим диагнозом крайне подвержены частым инфекциям, которые плохо поддаются лечению, длительно протекают, вызывают осложнения. Важно понимать, что здоровый ребенок также часто более простудами, что является вариантом нормы. Однако малыши с первичным иммунодефицитом страдают от них в разы чаще. При этом у них может одновременно протекать несколько инфекций, что наносит сильный удар ослабленному здоровью. На фоне этих проблем может возникать недостаточный набор веса, отставание роста, отклонения умственного развития.
Основными симптомами являются:
- Хронические инфекции с осложнениями
- Хронические кожные инфекции
- Хронические инфекции дыхательных путей
- Инфекции глаз
Диагностика и лечение
Диагноз ставится после проведения диагностического исследования гуморального и клеточного звеньев иммунитета. При подтверждении соответственной клинической картине пациенту назначается обследование крови. Детям в обязательном порядке проводится определение концентрации хлора в поте и функционирование поджелудочной железы, а также аллергопробы и ИФА. Как правило, этих данных достаточно для подтверждения диагноза.
В лечении первичного иммунодефицитного состояния применяется комплексный подход, который включает в себя:
- Своевременное устранение инфекционных очагов
- Оперативное вмешательство, направленное на замещение дефектного звена (иммуноглобулины, трансплантация костного мозга)
- Ферментативная терапия
- Цитокины
- Витаминно-минеральные комплекс
Видео о первичных иммуннодефицитах:
Вторичные иммунодефициты
В отличие от первого вида, они развиваются у людей с нормальной функционирующим от рождения иммунитетом. Их развитие происходит под воздействием внешних или внутренних факторов на уровне фенотипа. А также обусловлено нарушением работы иммунной системы вследствие разнообразных патологий или неблагоприятной окружающей среды (радиационное излучение и прочее). В этом случае поражаются Т- и В-ситсемы, факторы неспецифичной резистентности или их одновременная комбинация. Согласно медицинской статистике, вторичные иммунодефициты встречаются значительно чаще. Они имеют более благоприятный прогноз. Так как имеют переходящий характер и поддаются иммунокоррекции.
Причины возникновения вторичных иммунодецифитов
Среди возможных причин формирования этого состояния можно выделить:
- Перенесенные инфекции (особенно вирусного генеза) и инвазии (протозойные и гельминты)
- Ожоговая болезнь
- Злокачественные и доброкачественные новообразования
- Нарушение обмена веществ, истощение (недостаточное потребление продуктов питания)
- Дисбактериоз, тяжелые травмы
- Облучение, действий некоторых химических веществ
- Системные нарушения (сахарны диабет, ВИЧ и т.п.)
- Прием некоторых лекарственных препаратов и многое другое.
Диагностика и лечение
Для установки диагноза проводится тщательный осмотр пациента, собирается детальный анамнез (перенесенные недавно болезни, травмы и т.д.). Из лабораторных исследований назначается анализ крови и иммунограмма. Это иммунологические тесты, определяющие количественные и качественные характеристики составляющих элементов иммуннитета.
На наличие проблемы могут свидетельствовать как пониженные, так и повышенные показатели иммунограммы. Так как вторичный иммунодефицит хорошо поддается лечению, заболевания имеет благоприятный прогноз. В качестве терапии используется исключительно консервативная методика, подразумевающая прием медикаментов (иммуностимуляторов). Они назначаются для стимуляции активности неповрежденных звеньев иммунной системы, устранения дефектных участков цепи, включения в защиту резервных ресурсов и профилактики развития патологических реакций организма (аутоиммунные или аллергические).
Видео о вторичных иммуннодефицитах:
Ключевые моменты
- Расстройства иммунодефицита нарушают способность вашего организма защищаться от бактерий, вирусов и паразитов.
- Существует два типа нарушений иммунодефицита: те, с которыми вы родились (первичные), и те, которые приобретены (вторичные).
- Все, что ослабляет вашу иммунную систему, может привести к вторичному расстройству иммунодефицита.
Расстройства иммунодефицита защищают организм от инфекций и болезней.Этот тип расстройства облегчает заражение вирусами и бактериальными инфекциями.
Расстройства иммунодефицита являются врожденными или приобретенными. Врожденное или первичное расстройство - это то, с чем вы родились. Приобретенные или вторичные расстройства вы получаете позже в жизни. Приобретенные расстройства встречаются чаще, чем врожденные.
Ваша иммунная система включает в себя следующие органы:
Эти органы производят и выпускают лимфоциты. Это лейкоциты, классифицируемые как B-клетки и T-клетки.В и Т-клетки борются с захватчиками, называемыми антигенами. В-клетки выделяют антитела, специфичные для заболевания, которое выявляет ваш организм. Т-клетки разрушают чужеродные или аномальные клетки.
Примеры антигенов, которые могут понадобиться вашим В- и Т-клеткам, включают:
- бактерий
- вирусов
- раковых клеток
- паразитов
Расстройство иммунодефицита нарушает способность вашего организма защищаться от этих антигенов.
Иммунодефицитная болезнь возникает, когда иммунная система не работает должным образом.Если вы родились с дефицитом или у вас есть генетическая причина, это называется первичным иммунодефицитным заболеванием. Существует более 100 первичных нарушений иммунодефицита.
Примеры первичных иммунодефицитных расстройств включают в себя:
- Х-сцепленная агаммаглобулинемия (XLA)
- общий вариабельный иммунодефицит (CVID)
- тяжелый комбинированный иммунодефицит (SCID), который известен как синдром олимфоцитоза или «мальчик в пузыре»
Вторичные нарушения иммунодефицита случаются, когда на ваш организм нападает внешний источник, такой как токсичное химическое вещество или инфекция.Следующее может вызвать вторичное расстройство иммунодефицита:
Примеры вторичных расстройств иммунодефицита включают:
- СПИД
- раковых заболеваний иммунной системы, такие как лейкемия
- иммунно-комплексных заболеваний, таких как вирусный гепатит
- множественная миелома (рак плазматические клетки, которые продуцируют антитела)
Люди с семейной историей первичных нарушений иммунодефицита имеют более высокий, чем обычно, риск развития первичных нарушений.
Все, что ослабляет вашу иммунную систему, может привести к вторичному расстройству иммунодефицита. Например, причиной может быть воздействие жидкостей организма, инфицированных ВИЧ, или удаление селезенки.
Удаление селезенки может быть необходимо из-за таких состояний, как цирроз печени, серповидно-клеточная анемия или травма селезенки.
Старение также ослабляет вашу иммунную систему. По мере старения некоторые из органов, которые продуцируют лейкоциты, сжимаются и производят меньше их.
Белки важны для вашего иммунитета.Недостаточно белка в вашем рационе может ослабить вашу иммунную систему.
Ваше тело также производит белки во время сна, которые помогают организму бороться с инфекцией. По этой причине недостаток сна снижает вашу иммунную защиту. Раки и химиотерапевтические препараты также могут снизить ваш иммунитет.
Следующие заболевания и состояния связаны с первичными нарушениями иммунодефицита:
- атаксия-телеангиэктазия
- синдром Чедиака-Хигаси
- комбинированный иммунодефицитная болезнь
- дефицит комплемента
- синдром ДиДжорджа адгезия гипертензия
- гипертензия
- гипертензия
- гипертензия
- гипертензия
- гипертензия
- гипертензия
- гипертрофия дефекты
- пангипогаммаглобулинемия
- болезнь Брутона
- врожденная агаммаглобулинемия
- селективный дефицит IgA
- синдром Вискотта-Олдрича
Каждое расстройство имеет уникальные симптомы, которые могут быть частыми или хроническими.Некоторые из этих симптомов могут включать в себя:
Если эти проблемы не отвечают на лечение или вы не поправляетесь со временем, ваш врач может проверить вас на наличие иммунодефицитного расстройства.
Если ваш врач считает, что у вас может быть нарушение иммунодефицита, он захочет сделать следующее:
Вакцины могут проверить реакцию вашей иммунной системы в том, что называется тестом на антитела. Ваш доктор даст вам вакцину. Затем они проверит вашу кровь на ее реакцию на вакцину через несколько дней или недель.
Если у вас нет иммунодефицита, ваша иммунная система будет вырабатывать антитела для борьбы с организмами, содержащимися в вакцине. У вас может быть расстройство, если ваш анализ крови не показывает антитела.
Лечение для каждого нарушения иммунодефицита будет зависеть от конкретных условий. Например, СПИД вызывает несколько различных инфекций. Ваш врач назначит лекарства для каждой инфекции. Вам также может быть назначен антиретровирусный препарат и ВИЧ-инфекция, если это необходимо.
Лечение нарушений иммунодефицита обычно включает антибиотики и иммуноглобулиновую терапию. Другие противовирусные препараты, амантадин и ацикловир, или препарат под названием интерферон используются для лечения вирусных инфекций, вызванных нарушениями иммунодефицита.
Если ваш костный мозг не производит достаточное количество лимфоцитов, ваш врач может заказать пересадку костного мозга (стволовых клеток).
Первичные нарушения иммунодефицита можно контролировать и лечить, но их нельзя предотвратить.
Вторичные расстройства можно предотвратить несколькими способами. Например, можно предотвратить заражение СПИДом, не занимаясь незащищенным сексом с кем-то, кто заражен ВИЧ.
Сон очень важен для здоровой иммунной системы. По данным клиники Майо, взрослым нужно спать около восьми часов в сутки. Также важно, чтобы вы держались подальше от больных людей, если ваша иммунная система не работает должным образом.
Если у вас заразное иммунодефицитное заболевание, такое как СПИД, вы можете сохранить здоровье других, занимаясь безопасным сексом и не делясь с другими людьми, которые не заражены, телесными жидкостями.
Большинство врачей сходятся во мнении, что люди с нарушениями иммунодефицита могут вести полноценную и продуктивную жизнь. Раннее выявление и лечение расстройства очень важно.
Q:
У меня есть семейная история нарушений иммунодефицита. Если у меня есть дети, как рано они должны быть проверены на это?
A:
Семейный анамнез первичного иммунодефицита является самым сильным предиктором расстройства. При рождении и всего на несколько месяцев дети частично защищены от инфекций антителами, передаваемыми им матерями.Как правило, чем раньше возраст, в котором появляются признаки иммунодефицита у детей, тем тяжелее расстройство. Тестирование может быть проведено в течение первых нескольких месяцев, но также важно распознать ранние признаки: рецидивирующие инфекции и неспособность развиваться. Первоначальный лабораторный скрининг должен включать полный анализ крови с дифференциалом и измерением сывороточного иммуноглобулина и уровней комплемента.
Бренда Б. Сприггс, MD, FACP Ответы отражают мнение наших медицинских экспертов.Весь контент носит исключительно информационный характер и не должен рассматриваться как медицинский совет.Первичные иммунодефицитные заболевания (ПИ) - это группа из более чем 400 редких хронических заболеваний, при которых часть иммунной системы организма отсутствует или неправильно функционирует. Хотя эти заболевания не являются заразными, они вызваны наследственными или генетическими дефектами, и, хотя некоторые расстройства присутствуют при рождении или в раннем детстве, расстройства могут поражать любого, независимо от возраста или пола. Некоторые влияют на одну часть иммунной системы; другие могут влиять на один или несколько компонентов системы.И хотя болезни могут различаться, все они имеют одну общую черту: каждая из них является результатом нарушения одной из функций нормальной иммунной системы организма.
Поскольку одной из наиболее важных функций нормальной иммунной системы является защита нас от инфекции, пациенты с ПИ обычно имеют повышенную восприимчивость к инфекции. Инфекции могут быть в коже, пазухах, горле, ушах, легких, головном или спинном мозге или в мочевых или кишечных трактах, а повышенная уязвимость к инфекции может включать повторные инфекции, инфекции, которые не будут устранение или необычно тяжелые инфекции.Люди с ИП живут всю свою жизнь, более восприимчивые к инфекциям - они испытывают постоянные проблемы со здоровьем и часто развивают серьезные и изнурительные заболевания. К счастью, при надлежащем медицинском обслуживании многие пациенты живут полноценной и независимой жизнью.
Это просто инфекция?
Вы должны быть подозрительны, если у вас есть инфекция, которая ...
- Тяжелый - требует госпитализации или внутривенного введения антибиотиков
- Постоянный - не очищается полностью или очищается очень медленно
- Необычный - вызванный необычным организмом
- Recurrent - продолжает возвращаться или если это
- Бег в семье - у других в вашей семье была похожая подверженность инфекции
- Если какое-либо из этих слов описывает вашу инфекцию, Фонд иммунодефицита (IDF) рекомендует вам попросить вашего врача проверить возможность возникновения PI.Нажмите здесь, чтобы узнать больше о конкретных типах ПИ. Если у вас есть дополнительные вопросы, пожалуйста, свяжитесь с IDF через Ask IDF или позвоните по телефону 800-296-4433.
| х | х | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ИНФЕКЦИОННЫЙ БОЛЕЗНЬ | БАКТЕРИОЛОГИЯ | ИММУНОЛОГИЯ | МИКОЛОГИЯ | ПАРАЗИТОЛОГИЯ | ВИРОЛОГИЯ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FRANCAIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ТУРЕЦКИЙ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Дайте нам знать, что вы думаете ОБРАТНАЯ СВЯЗЬ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ПОИСК | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изображение логотипа Джеффри Нельсон, Университет Раша, Чикаго, Иллинойс и MicrobeLibrary | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ОБУЧЕНИЕ ЗАДАЧИ Познай первичные и вторичные иммунодефициты Знать иммунодефициты при СПИДе и другие состояния | ИММУНОДЕФИКАЦИЯ Иммунодефицит неспособность иммунной системы защитить от болезней или злокачественных новообразований. Первичный иммунодефицит вызван генетическими или пороками развития в иммунной системе. Эти дефекты присутствуют при рождении, но могут проявиться позже в жизни. Вторичным или приобретенным иммунодефицитом является потеря иммунная функция в результате воздействия возбудителей болезней, окружающей среды факторы, иммуносупрессия или старение. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Знай майор первичные иммунодефициты и их особенности Понять связь между местом поражения и возникающим иммунодефицитом Познай диагностические тесты на разные иммунодефициты
|
ПЕРВИЧНЫЙ ИММУНОДЕФИКАЦИЯ Первичные иммунодефициты наследственные дефекты иммунной системы (рисунок 1).Эти дефекты могут быть в специфические или неспецифические иммунные механизмы. Они классифицированы на Основа сайта поражения в развитии или дифференцировке путь иммунной системы. лиц с иммунодефициты подвержены различным инфекциям и типу инфекции зависит от характера иммунодефицита (таблица 1).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рисунок 1 Пороки развития при первичных иммунодефицитах | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Специфическая иммунная система Есть множество иммунодефициты, возникающие в результате дефектов дифференцировки стволовых клеток и может включать Т-клетки, В-клетки и / или иммуноглобулины разных классы и подклассы (Таблица 2). Дефект раннего кроветворения который включает в себя стволовые клетки приводит к ретикулярной дисгенезия, который приводит к общие иммунные дефекты и последующая подверженность инфекциям. это состояние часто смертельно, но очень редко. Это можно успешно лечить пересадка костного мозга.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| Расстройства Т клетки Т-клеточные нарушения влияют как на клеточные, так и на гуморальный иммунитет делает пациента восприимчивым к вирусным, простейшим и грибковая инфекция.Вирусные инфекции, такие как цитомегаловирус и ослабленная корь в вакцине может быть смертельным для этих пациентов.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ДЕЛО ПРЕЗЕНТАЦИЯ педиатрический Патология | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рисунок 2 При синдроме ДиДжорджа, 22q11.2 делеция наследуется в аутосомно доминирующая картина. Национальная медицинская библиотека - NIH Рисунок 3 | Т-клеточных дефицитов с переменная степень дефицита B-клеток
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рис. 4 Синдром Вискотта-Олдрича - это расстройство, связанное с Х. Национальная медицинская библиотека - NIH | Расстройства лимфоцитов B Есть ряд заболеваний в котором номера и функции T-ячеек нормальные: номера B-ячеек могут быть низкий или нормальный, но уровень иммуноглобулина низкий.
Х-сцепленная гипогаммаглобулинемия, также называемая гипоглобулинемией Брутона или агаммаглобулинемия, самая тяжелая гипогаммаглобулинемия, при которой В количество клеток и все уровни иммуноглобулина очень низки. Пациенты имеют сбой созревания В-клеток, связанный с дефектом В-клеток ген тирозинкиназы ( btk ). Таким образом, В-клетки существуют в виде пре-В-клеток с H цепи, но не L цепи переставляются.Диагноз основывается на перечислении В-клеток и измерение иммуноглобулина. У пациентов нет иммуноглобулины и страдают от повторяющихся бактериальных инфекций. Временная гипогаммаглобулинемия Общая переменная гипогаммаглобулинемия (поздняя гипогаммаглобулинемия) IgA дефицит Избирательный дефицит IgG Х-сцепленный гипер-IgM иммунодефицит
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рисунок 5 Плохое внутриклеточное уничтожение бактерий при хроническом гранулематозная болезнь
| Неспецифическая иммунная система - ДЕФЕКТЫ В МИЕЛОИДНОЙ ЛИНИИ Первичные иммунодефициты неспецифическая иммунная система включает дефекты фагоцитов и NK-клеток и система дополнения.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Рисунок 6 Этот слайд из пациент с синдромом Чедьяка-Хигаси. Чрезвычайно большие гранулы видны в цитоплазма гранулоцитов. Они являются результатом ненормального слияния гранул во время их формирования. Аномальные гранулы обнаружены во многих других клетках типы по всему телу Национальный институт рака |
При этом заболевании Т-клетки и макрофаги лишены рецептора комплемента CR3 из-за дефекта в CD11 или Пептиды CD18 и, следовательно, они не могут отвечать на опсонин C3b.В качестве альтернативы может присутствовать дефект в молекулах интегрина, LFA-1 или mac-1. возникающие из дефектных пептидов CD11a или CD11b соответственно. Эти молекулы участвуют в диапедез и, следовательно, дефектные нейтрофилы не может эффективно реагировать на хемотаксические сигналы. Лечение с костный мозг (лишенный Т-клеток и соответствующих МНС) трансплантация или ген терапия. Синдром Чедьяка-Хигаси
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Расстройства системы комплемента дополняют аномалии также привести к повышенной восприимчивости к инфекциям. Есть генетические Недостатки различных компонентов системы комплемента, наиболее серьезные из которых дефицит С3 которые могут возникнуть из-за низкого синтеза C3 или дефицита фактора I или фактора ЧАС. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ВТОРИЧНЫЕ (ПРИОБРЕТЕННЫЕ) ИММУНОДЕФИКАЦИИ Иммунодефициты, связанные с инфекциями Иммунологические нарушения в СПИД
Иммунодефициты, связанные со старением
Иммунодефициты, связанные со злокачественными новообразованиями и другими заболеваниями Другие условия, при которых возникают вторичные иммунодефициты: серповидноклеточная анемия, диабет сахар, белковая недостаточность калорий, ожоги, алкогольный цирроз, ревматоидный артрит, почечная недостаточность, и др. .
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



