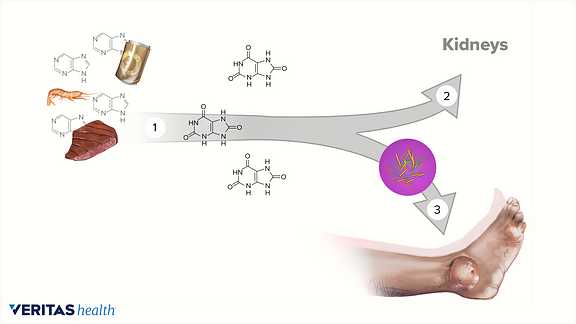
Какие продукты образуются при полном и неполном сгорании сероводорода
Составьте уравнения реакций полного и неполного сгорания
Составьте уравнения окислительно-восстановительных реакций полного и неполного сгорания сероводорода. Укажите окислитель и восстановитель.
Ответ| Неполное сгорание сероводорода 2H2S + O2 ⟶ 2H2O + 2S |
||
| O20 + 4ē ⟶ 2O-2 | 1 | окислитель (восстановление) |
| S-2 - 2ē ⟶ S0 | 2 | восстановитель (окисление) |
| Полное сгорание сероводорода 2H2S + 3O2 ⟶ 2H2O + 2SO2 |
||
| O20 + 4ē ⟶ 2O-2 | 3 | окислитель (восстановление) |
| S-2 - 6ē ⟶ S+4 | 2 | восстановитель (окисление) |
gomolog.ru1https://gomolog.ru/reshebniki/9-klass/rudzitis-i-feldman-2019/19/zadanie-1.html
gomolog.ru11https://gomolog.ru/reshebniki/9-klass/rudzitis-i-feldman-2019/19/zadanie-1.html
Учебное пособие по химии сжигания углеводородов
Пожалуйста, не блокируйте рекламу на этом сайте.
Без рекламы = для нас нет денег = для вас нет бесплатных вещей!
Полное сжигание углеводородов
Любой углеводород сгорает в избытке кислорода с образованием газообразного диоксида углерода и водяного пара.
Для полного сгорания углеводорода:
⚛ газообразный кислород - избыток реагента
⚛ углеводород - ограничивающий реагент
Мы можем написать общее словесное уравнение для полного сгорания любого углеводорода, как показано ниже:
углеводород + избыточный газообразный кислород → газообразный диоксид углерода + водяной пар
Углеводороды включают алканы, алкены и алкины, поэтому мы можем сказать, что:
⚛ любой алкан сгорает в избытке кислорода с образованием газообразного диоксида углерода и водяного пара
алкан + избыток газообразного кислорода → газообразный диоксид углерода + водяной пар
⚛ любой алкен сгорает в избытке кислорода с образованием газообразного диоксида углерода и водяного пара
алкен + избыток газообразного кислорода → газообразный диоксид углерода + водяной пар
⚛ любой алкин сгорает в избытке кислорода с образованием газообразного диоксида углерода и водяного пара
алкин + избыток газообразного кислорода → газообразный диоксид углерода + водяной пар
Пример: полное сгорание метана
Метан, CH 4 (г) , представляет собой углеводород.Это соединение, состоящее только из элементов углерода (C) и водорода (H).
Метан - это газ при комнатной температуре и давлении. Это обычный компонент природного газа, который используется в качестве топлива.
Метан сгорает в избытке кислорода с образованием газообразного диоксида углерода (CO 2 (г) ) и водяного пара (H 2 O (г) ).
Сгорание с избытком кислорода называется полным сгоранием.
Мы можем написать сбалансированное химическое уравнение для представления полного сгорания газообразного метана, как показано ниже:
- Напишите словесное уравнение для полного сгорания метана:
общее уравнение: реактивы → товаров слово уравнение: метан + газообразный кислород → углекислый газ + водяной пар - Запишите молекулярную формулу для каждого реагента и продукта в словесном уравнении:
Реагенты Продукты метан: газообразный кислород:
CH 4 (г) O 2 (г)
углекислый газ: водяной пар:
CO 2 (г) H 2 O (г)
- Напишите несбалансированное химическое уравнение, подставив молекулярную формулу для названия каждого реагента и продукта в словесное уравнение:
общее уравнение: реактивы → товаров уравнение слова: метан + газообразный кислород → углекислый газ + водяной пар несбалансированное химическое уравнение: CH 4 (г) + O 2 (г) → CO 2 (г) + H 2 O (г) - Уравновесить химическое уравнение:
несбалансированное химическое уравнение: CH 4 (г) + O 2 (г) → CO 2 (г) + H 2 O (г) No.Атомы C: 1 = 1 C-атомы сбалансированы Кол-во атомов H: 4 ≠ 2 Атомы H НЕ сбалансированы Необходимо умножить количество молекул воды на 2 , чтобы уравновесить атомы водорода.Затем проверьте баланс этого нового химического уравнения, как показано ниже. CH 4 (г) + O 2 (г) → CO 2 (г) + 2 H 2 O (г) Кол-во атомов C: 1 = 1 C-атомы сбалансированы No.Атомы H: 4 = 4 Сбалансированные атомы H Кол-во атомов O: 2 ≠ 2 + 2 Атомы O НЕ сбалансированы Необходимо умножить количество молекул кислорода на 2 , чтобы уравновесить атомы кислорода.Затем проверьте баланс этого нового химического уравнения, как показано ниже: CH 4 (г) + 2 O 2 (г) → CO 2 (г) + 2H 2 O (г) Кол-во атомов C: 1 = 1 C-атомы сбалансированы No.Атомы H: 4 = 4 Сбалансированные атомы H Кол-во атомов O: 4 = 2 + 2 Атомы О сбалансированы - Сбалансированное химическое уравнение полного сгорания газообразного метана:
CH 4 (г) + 2O 2 (г) → CO 2 (г) + 2H 2 O (г)
Неполное сжигание углеводородов
Если присутствует недостаточно газообразного кислорода для сгорания углеводорода, чтобы произвести наиболее окисленную форму углерода, которой является газообразный диоксид углерода, мы называем реакцию неполным сгоранием углеводорода.
Для неполного сгорания углеводорода:
⚛ газообразный кислород - ограничивающий реагент
⚛ углеводород - избыток реагента
Неполное сгорание углеводорода обычно приводит к возникновению «сажистого» пламени из-за присутствия углерода (C) или сажи как продукта реакции неполного сгорания.
Водород в углеводороде будет окислен до воды, H 2 O, но углерод в углеводороде может или не может быть окислен до газообразного монооксида углерода (CO (г) ).
Пример: неполное сгорание метана
В конкретном эксперименте избыточный газообразный метан (CH (g) ) сжигался в ограниченном количестве газообразного кислорода с образованием сажи (твердого углерода) и водяного пара.
Мы можем написать сбалансированное химическое уравнение, чтобы представить это неполное сгорание метана в этом эксперименте, как показано ниже:
- Напишите уравнение неполного сгорания метана в словах:
общее уравнение: реактивы → товаров слово уравнение: метан + газообразный кислород → твердый углерод + водяной пар - Запишите молекулярную формулу для каждого реагента и продукта в словесном уравнении:
Реагенты Продукты метан: газообразный кислород:
CH 4 (г) O 2 (г)
твердый углерод: водяной пар:
C (с) H 2 O (г)
- Напишите несбалансированное химическое уравнение, подставив формулу для названия каждого реагента и продукта в словесное уравнение:
общее уравнение: реактивы → товаров слово уравнение: метан + газообразный кислород → твердый углерод + водяной пар несбалансированное химическое уравнение: CH 4 (г) + O 2 (г) → C (т) + H 2 O (г) - Уравновесить химическое уравнение:
несбалансированное химическое уравнение: CH 4 (г) + O 2 (г) → C (т) + H 2 O (г) No.Атомы C: 1 = 1 C-атомы сбалансированы Кол-во атомов H: 4 ≠ 2 Атомы H НЕ сбалансированы Необходимо умножить количество молекул воды на 2 , чтобы уравновесить атомы водорода.Затем проверьте баланс нового уравнения: CH 4 (г) + O 2 (г) → C (т) + 2 H 2 O (г) Кол-во атомов C: 1 = 1 C-атомы сбалансированы No.Атомы H: 4 = 4 Сбалансированные атомы H Кол-во атомов O: 2 = 2 Атомы О сбалансированы - Уравновешенное химическое уравнение неполного сгорания газообразного метана в этом эксперименте имеет следующий вид:
CH 4 (г) + O 2 (г) → C (с) + 2H 2 O (г)
Сероводород - Simple English Wikipedia, бесплатная энциклопедия
| | |||
| Имена | |||
|---|---|---|---|
| Систематическое наименование ИЮПАК | |||
Другие наименования
| |||
| Идентификаторы | |||
| 3DMet | {{{value}}} | ||
| Beilstein Ссылка | 3535004 | ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.070 | ||
| Номер ЕС | 231-977-3 | ||
| Gmelin Ссылка | 303 | ||
| КЕГГ | |||
| MeSH | {{{value}}} | ||
| PubChem | {{{value}}} | ||
| Номер RTECS | MX1225000 | ||
| UNII | |||
| Номер ООН | 1053 | ||
| УЛЫБКИ | {{{value}}} | ||
| Недвижимость | |||
| H 2 S | |||
| Молярная масса | 34.08 г · моль -1 | ||
| Внешний вид | Бесцветный газ | ||
| Запах | Тухлые яйца | ||
| Плотность | 1,363 г дм −3 | ||
| Температура плавления | -82 ° С (-116 ° F, 191 К) | ||
| Температура кипения | -60 ° С (-76 ° F, 213 К) | ||
| 4 г дм −3 (при 20 ° C) | |||
| Давление пара | 1740 кПа (при 21 ° C) | ||
| Кислотность (p K a ) | 7.0 [2] [3] | ||
| Конъюгированная кислота | сульфоний | ||
| Основание конъюгата | Бисульфид | ||
| −25,5 · 10 −6 см 3 / моль | |||
| 1.000644 (0 ° C) [4] | |||
| Структура | |||
| C 2v | |||
| Бент | |||
| 0.97 D | |||
| Термохимия | |||
| Стандартная энтальпия образования Δ f H | −21 кДж моль −1 [5] | ||
| Стандартная мольная энтропия S | 206 Дж моль −1 K −1 [5] | ||
| Удельная теплоемкость, C | 1.003 J K −1 g −1 | ||
| Опасности | |||
| Классификация ЕС | Факс: + Тел .: + N | ||
| Основные опасности | Легковоспламеняющийся и высокотоксичный | ||
| NFPA 704 |
4 4 0
| ||
| R-фразы | R12 , R26 , R50 | ||
| S-фразы | (S1 / 2) , S9 , S16 , S36 , S38 , S45 , S61 | ||
| Пределы взрываемости | 4.3–46% | ||
| Допустимый предел воздействия США (PEL) | C 20 частей на миллион; 50 частей на миллион [максимум 10 минут] | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| N проверить (что такое YN ?) | |||
| Ссылки на инфобокс | |||
Сероводород (британский английский: сероводород ) - химическое соединение с формулой H
2 S, бесцветный, токсичный, легковоспламеняющийся газ, вызывающий неприятный запах гнили. яйца и метеоризм.Часто это происходит, когда бактерии расщепляют органические вещества при отсутствии кислорода. Это происходит и в болотах, и в канализации (параллельно с процессом анаэробного пищеварения). Это также происходит в вулканических газах, природном газе и некоторых скважинных водах. Это запах, который люди часто принимают за запах серы. Но сама сера не пахнет.
Сероводород также известен как сульфан , сероводород , высокосернистый газ , сероводород , сероводородная кислота , канализационный газ и вонь .ИЮПАК принимает названия «сероводород» и «сульфан». Когда люди говорят о более сложных соединениях, они всегда используют термин «сульфан».
Отложение серы на скале, вызванное вулканическими газами, содержащими сероводород.Небольшие количества сероводорода можно найти в сырой нефти. Кислый природный газ может содержать до 28%. Но высокосернистый природный газ необходимо очищать, прежде чем он попадет в магистральный трубопровод. Трубопроводы ограничивают содержание сероводорода до 3 гран на тысячу кубических футов природного газа. [6] Вулканы и горячие источники выделяют некоторое количество H 2 S, где он, вероятно, образуется в результате гидролиза сульфидных минералов, т.е. MS + H 2 O с образованием MO + H 2 S.
Нормальная средняя концентрация в чистом воздухе составляет около 0,0001-0,0002 ppm.
Сероводород - высокотоксичный и легковоспламеняющийся газ. Поскольку он тяжелее воздуха, он имеет тенденцию скапливаться на дне плохо вентилируемых помещений.
Сероводород считается ядом широкого спектра действия, что означает, что он может отравить несколько различных систем организма, хотя больше всего страдает нервная система.Токсичность H 2 S сопоставима с токсичностью цианистого водорода.
- ↑ «Сероводород - публичная химическая база данных PubChem». Проект PubChem . США: Национальный центр биотехнологической информации.
- ↑ Перрин, Д.Д. (1982). Константы ионизации неорганических кислот и оснований в водном растворе (2-е изд.). Оксфорд: Pergamon Press.
- ↑ Bruckenstein, S .; Kolthoff, I.M., в Kolthoff, I.M.; Elving, P.J. Трактат по аналитической химии , Vol. 1, пт. 1; Wiley, NY, 1959 , стр. 432–433.
- ↑ Патнаик, Прадёт (2002). Справочник по неорганическим химическим веществам . Макгроу-Хилл. ISBN 0-07-049439-8 .
- ↑ 5,0 5,1 Зумдал, Стивен С. (2009). Химические принципы (6-е изд.). Компания Houghton Mifflin. п. A23. ISBN 0-618-94690-X .
- ↑ "Тарифы Южной природной газовой компании, Общие положения и условия Раздел 3.1 (b) ". Проверено 18 октября 2011 г..
- «Сероводород», Комитет по медицинским и биологическим эффектам загрязнителей окружающей среды, University Park Press, 1979, Балтимор. ISBN 0-8391-0127-9
вопросов и ответов по газу
Прочтите следующие вопросов и ответов по газу , таким как метан, пропан, оксид углерода, оксиды азота, водород, кислород, азот, диффузия газов, диоксид углерода, диоксид серы, сероводород и т. Д.
Вопросы и ответы по газу
Метан
Каков удельный вес метана?
0,5545.
Какой химический символ у метана?
Ч5.
Где метан наиболее вероятно можно найти в шахте?
Рядом с крышей, так как она легче воздуха.
Что представляет собой легковоспламеняющаяся смесь метана и воздуха, которая может гореть или взорваться при возгорании?
Firedamp
Какая температура воспламенения метана?
1100 ° - 1380 ° F.
Какие инструменты чаще всего используются для обнаружения метана?
Лампа безопасности пламени и детекторы метана.
Какой наименьший процент метана может быть обнаружен с помощью пламегасителя?
Около одного процента (1%).
Как присутствие метана влияет на взрывоопасность угольной пыли?
Угольная пыль легче воспламеняется, и сила взрыва больше.
Как угольная пыль в воздухе влияет на взрывоопасность метана?
Нижний предел взрываемости снижен.
С каким опасным газом наиболее вероятно столкнуться при падении колонны?
Метан.
Как присутствие метана влияет на взрывоопасность угольной пыли?
Угольная пыль легче воспламеняется, и сила взрыва больше.
Как угольная пыль в воздухе влияет на взрывоопасность метана?
Нижний предел взрываемости снижен.
С каким опасным газом наиболее вероятно столкнуться при падении столба (шахты)?
Метан.
Почему метан будет скапливаться в недостаточно вентилируемом месте?
Он легче воздуха и будет подниматься и расслаиваться, если не распределять должным образом.
Какой в основном горючий газ обычно находится в угольных шахтах?
Метан.
Ядовит ли метан (Ch5)?
№
Какого цвета метан?
Метан бесцветен.
Что самое тяжелое: один кубический фут метана или один кубический фут воздуха?
Один кубический фут воздуха.
Какой газ находится возле кровли и впадин на водопадах?
Метан (Ч5).
Какой газ без запаха, вкуса, нетоксичен, бесцветен и взрывоопасен в концентрации 5-15%?
Метан
Что является источником метана в угольных шахтах?
Освобожден от угля и прилегающих пластов.
Где обычно находится метан в шахтах?
Вдоль кровли, до подъемов, в районе рабочих забоев, в тупиках и выше водопадов.
Является ли метан взрывчатым веществом?
Нет. Кислород необходим для поддержания горения.
Почему не может быть взрыва, если процентное содержание метана превышает пятнадцать процентов (15%)?
Поскольку количество присутствующего кислорода недостаточно для быстрого сгорания.
Как можно обнаружить газообразный метан в угольной шахте?
Химический анализ, пламегаситель и детекторы метана.
Каков взрывоопасный диапазон метана?
От пяти до пятнадцати процентов.
Какой процент метана требуется для максимальной взрывоопасности?
Десять процентов (10%).
Каков вес одного кубического фута метана при 60 градусах по Фаренгейту и 30,00 дюймах ртутного столба?
Четыреста двадцать четыре десятитысячных одного фунта (0.0424).
Окись углерода
Какой процент окиси углерода может вызвать смерть менее чем за час?
0,4 процента или более.
Какая температура воспламенения окиси углерода?
1100 ° F.
Почему небольшие количества окиси углерода опасны?
Потому что он нелегко выводится и накапливается в крови.
Какой химический символ у окиси углерода?
CO.
Каков удельный вес окиси углерода?
0,967.
Что такое окись углерода (CO)?
Это бесцветный, без запаха, вкуса, горючий и ядовитый газ.
Как можно обнаружить окись углерода?
Детекторами угарного газа и химическим анализом.
Запрещается использовать рабочих в течение 8 часов, если содержание окиси углерода превышает какое?
50 частей на миллион (0.005%).
Какой процент окиси углерода может вызвать симптомы отравления, если дышать бесконечно долго?
0,01% (100 частей на миллион).
Что является источником окиси углерода?
Это продукт неполного сгорания (сгорание при недостатке кислорода).
Когда окись углерода наиболее вероятно может быть обнаружена в шахтах?
При пожаре на мине или после взрыва.
На что указывает присутствие CO в закрытой шахте?
Пожар.
Какой процент насыщения крови оксидом углерода (CO) приведет к смерти?
70% - 80%.
Какой взрывоопасный диапазон окиси углерода?
12,5% - 74%.
Какой процент оксида углерода вызовет легкие симптомы через несколько часов?
200 частей на миллион (0,02%).
Какой процент окиси углерода вызовет дискомфорт через два или три часа?
400 частей на миллион (0,04%).
Какой процент оксида углерода вызывает тенденцию к шатанию через полтора (1½) часа?
1200 частей на миллион (0.12%).
Какой процент окиси углерода вызовет симптомы потери сознания через тридцать (30) минут?
2000–2500 частей на миллион (0,20–0,25%).
Насколько большее сродство гемоглобина к окиси углерода, чем к кислороду?
Примерно 300 (триста) раз.
Какой ядовитый газ выделяется в основном при взрывах?
Окись углерода.
Какое влияние окись углерода оказывает на жизнь?
Он очень ядовит.
Как окись углерода причиняет вред жизни?
Путем объединения с гемоглобином крови и без кислорода.
Каков вес одного (1) локтевого фута окиси углерода при 60 градусах по Фаренгейту и 30,00 дюймах ртутного столба?
Семьсот сорок десять тысячных одного фунта (0,0740).
Оксиды азота
Как образуются оксиды азота?
От использования взрывчатых веществ в шахтах.
Как оксиды азота вызывают смерть?
Вызывает скопление жидкости в легких, что приводит к асфиксии.
Как сообщаются результаты анализа оксидов азота?
В пересчете на диоксид азота.
Какой химический символ у диоксида азота?
НО2.
Укажите пороговое значение для оксидов азота.
5 частей на миллион (0,0005%).
Каков удельный вес диоксида азота?
1.589.
Каков удельный вес оксида азота?
1.036.
Каков вес кубического фута перекиси азота при 60 градусах по Фаренгейту и 30,00 дюймах ртутного столба?
Двенадцатьсот семнадцать десятитысячных (0,1217) одного фунта.
Водород
Каков удельный вес водорода?
Это самый легкий из газов с удельным весом 0,0695
Какой химический символ у водорода?
h3.
Какие источники водорода в шахте?
Зарядка аккумуляторов, горение мин и взрывы.
После какого взрыва всегда присутствует водород?
Взрывы угольной пыли.
Взрывоопасен ли водород?
Да.
Назовите газ, который вырабатывается аккумуляторной батареей.
Водород (h3).
Каков взрывоопасный диапазон водорода?
4,0% - 74,2% при наличии всего 5% кислорода.
Как определяется водород?
Путем химического анализа.
Горюч ли водород?
Да.
Растворим ли водород в воде?
№
Какая концентрация вызывает самый сильный взрыв?
Очень сильные взрывы возможны, если в воздухе содержится более 7-8 процентов водорода.
Может ли водород влиять на взрывоопасный диапазон других газов?
Да, присутствие небольшого количества водорода значительно увеличивает взрывоопасный диапазон других газов.
Каков вес одного кубического фута водорода при 60 градусах по Фаренгейту и 30,00 дюймах ртутного столба?
г. Пятьдесят три десятитысячных (0,0053) одного фунта.
Разное
Запишите химические символы метана и сероводорода.
Ch5 и h3S
Назовите невзрывоопасные газы в угольных шахтах.
Двуокись углерода (CO2) и азот (N2)
Назовите взрывоопасные газы, обнаруженные в каменноугольных шахтах.
Метан (Ch5), окись углерода (CO) и сероводород (h3S).
Что такое TLV?
Пороговое предельное значение.
Преобразование 0,01 процента окиси углерода в ppm.
100 частей на миллион.
Что такое ядовитый газ?
Любой газ в воздухе, который опасен для жизни при вдыхании.
Какое процентное содержание кислорода, ниже которого не может произойти взрыва воздушной смеси метана?
12%.
Какое влияние оказывает атмосфера с пониженным содержанием кислорода на взрывоопасность метана?
Для начала взрыва в атмосфере, содержащей менее чем нормальный процент кислорода, необходимо большее количество метана.
Кислород
Каков удельный вес кислорода?
1.105.
Какой химический символ у кислорода?
O2.
Какой процент атмосферы Земли составляет кислород?
20,94% кислорода.
В закрытой зоне угольной шахты по прошествии некоторого времени будет обнаружено отсутствие чего?
Кислород.
Возможен ли пожар на шахте или взрыв без кислорода?
№
Кислород легковоспламеняющийся или взрывоопасный?
Нет, сам по себе кислород не горит и не взрывается, он просто поддерживает горение. Однако атмосфера, обогащенная кислородом, наряду с наличием воспламенения горючего материала будет вызывать чрезвычайно быстрое горение и в некоторых случаях вспышку, что увековечивает миф о том, что кислород является горючим и взрывоопасным.
Шахтный воздух не должен содержать меньше, чем процент кислорода?
19,5%.
Как организм получает кислород?
При дыхании кислород поглощается гемоглобином крови и переносится во все части тела.
Что поддерживает химическую реакцию, приводящую к пожарам и взрывам?
Кислород.
С каким процентом кислорода человеку легче всего работать?
20,9%.
С каким процентным содержанием кислорода человек будет дышать быстрее и глубже во время работы?
17%.
Лампа безопасности пламени гаснет, когда процентное содержание кислорода ниже какого?
16%.
Какой элемент в воздухе необходим для жизни?
Кислород.
Как организм получает кислород?
При дыхании кислород поглощается кровью и переносится к клеткам тела.
Когда уровень кислорода (O2) в воздухе считается опасным?
Когда уровень кислорода (O2) падает ниже 16%.
Азот
Каков удельный вес азота?
0,967.
Какой процент атмосферы Земли состоит из азота?
78.09% азота.
Какой химический символ у азота?
N2.
Какое пороговое значение азота?
81%.
Что такое азот?
Это газ без вкуса, запаха и цвета, который не поддерживает ни жизнь, ни горение.
Горюч ли азот?
№
Какое влияние оказывает азот на распространение взрыва?
Нет.
Как азот влияет на жизнь?
Не имеет никакого эффекта, за исключением случаев, когда он истощает кислород до такой степени, что возникает дефицит кислорода.
Есть ли у азота температура воспламенения?
Нет, азот не взорвется.
Каков вес одного (1) кубического фута азота при 60 градусах по Фаренгейту и 30,00 ртутного давления?
Семьсот пятьдесят десять тысячных одного фунта (0,0750).
Диффузия газов
При однородном смешивании двух или более газов они разделятся или распадутся?
№
Дайте определение термину диффузия газов.
Диффузия - это явление, при котором газы смешиваются под действием естественных сил.
Что такое закон диффузии?
Скорость диффузии обратно пропорциональна квадратному корню из удельного веса.
Что такое стратификация?
Когда газы не диффундируют полностью, слои газа расслаиваются по горизонтали.
В какой атмосфере легко обнаружить газ: диффузная или стратифицированная?
Стратифицированный.
Двуокись углерода
Горюч ли углекислый газ?
№
Каков удельный вес двуокиси углерода?
1,529.
Какой химический символ у двуокиси углерода?
CO2.
Где обычно можно найти концентрированные скопления двуокиси углерода?
Возле пола, в плохо проветриваемых местах.
Какое влияние оказывает углекислый газ на жизнь?
Дыхание увеличивается по мере увеличения концентрации углекислого газа.
Как определяется углекислый газ?
Обычно химическим анализом.
Что такое диоксид углерода (CO2)?
Двуокись углерода - это бесцветный газ без запаха, образованный химической комбинацией углерода и кислорода.
Как углекислый газ образуется в шахте?
Путем сжигания, дыхания шахтеров и животных, разложения растительных и животных материалов, окисления угля и химического воздействия кислой воды на карбонаты.
Что такое продукт полного сгорания?
Двуокись углерода.
Где обычно можно найти концентрированные скопления двуокиси углерода?
Возле пола, в плохо проветриваемых местах.
Какое влияние оказывает углекислый газ на жизнь?
Дыхание увеличивается по мере увеличения концентрации углекислого газа.
Как определяется углекислый газ?
Обычно химическим анализом. Однако в плохо вентилируемых зонах шахты повышенный уровень CO2 будет присутствовать при обнаружении низкого содержания кислорода.
Как углекислый газ образуется в шахте?
Путем сжигания, дыхания шахтеров и животных, разложения растительных и животных материалов, окисления угля и химического воздействия кислой воды на карбонаты.
Что такое продукт полного сгорания?
Двуокись углерода.
Каков вес одного (1) кубического фута углекислого газа при 60 градусах по Фаренгейту и 30,00 дюймах ртутного столба?
Одиннадцатьсот семьдесят десять тысячных (0.1170) фунтов.
Диоксид серы
Как диоксид серы образуется в шахте?
Путем сжигания угля, содержащего колчедан.
Каков удельный вес диоксида серы?
2,263.
Какой химический символ у диоксида серы?
SO2.
В чем особая опасность диоксида серы?
Он чрезвычайно ядовит даже в небольших количествах.
Как определяется диоксид серы?
По обонянию и его влиянию на дыхательные пути.
Каков первый эффект на человека, подвергшегося воздействию двуокиси серы?
Он вызывает сильное раздражение, удушье и невыносимо для дыхания.
Горюч ли диоксид серы?
Нет, негорючий.
Растворим ли диоксид серы в воде?
Да.
Каков вес кубического фута диоксида серы при 60 градусах по Фаренгейту и 30,00 дюймах ртутного столба?
Семнадцатьсот тридцать три десятитысячных (0.1733) фунт.
Сероводород
Каков удельный вес сероводорода?
1,191.
Какой химический символ у сероводорода?
х3С.
Каковы свойства сероводорода?
Ядовитый и бесцветный с запахом тухлых яиц.
Какой шахтный газ можно определить по запаху?
Сероводород.
Каково происхождение сероводорода?
Он выделяется при сжигании взрывчатых веществ, содержащих серу, таких как черный порох или динамит.
Как можно определить сероводород помимо обоняния?
Детектором сероводорода или бумагой, смоченной ацетатом свинца, который сразу же станет черным при воздействии сероводорода.
Каким характерным запахом пахнет газообразный сероводород?
Пахнет тухлыми яйцами.
Каков взрывоопасный диапазон сероводорода?
4,3% - 45%.
Ядовит ли сероводород?
Да, даже в небольших количествах он очень ядовит.
Были ли случаи гибели людей на шахтах в результате отравления сероводородом?
Определенно да. Две самые известные аварии, связанные с отравлением h3S, произошли на руднике Barnett Complex в 1971 году и на руднике Sullivan (Канада) в 2006 году. Шахта Barnett была рудной шахтой. Салливан был свинцово-цинковым рудником.
Каков непосредственный эффект от сероводорода на человека?
Сильно раздражает глаза.
Какое пороговое значение для сероводорода?
10 частей на миллион (0.0001%).
Какой из метана, окиси углерода и сероводорода имеет самую низкую температуру воспламенения?
Сероводород (700 ° F).
Каков вес одного (1) кубического фута сероводорода при 60 градусах по Фаренгейту и 30,0 0 дюймах ртутного столба?
Девятьсот одиннадцать десятитысячных (0,0911) фунта.
Также читайте: Принцип работы выталкивающего барабана для факелов
.6.6: Объемы газа и стехиометрия
Пример 6.6.1
Серная кислота, промышленный химикат, производимый в наибольшем количестве (почти 45 миллионов тонн в год только в Соединенных Штатах), получается путем сжигания серы на воздухе с образованием SO 2 с последующей реакцией SO 2 с O 2 в присутствии катализатора с образованием SO 3 , который реагирует с водой с образованием H 2 SO 4 . Общее химическое уравнение выглядит следующим образом:
\ [\ rm 2S _ {(s)} + 3O_ {2 (g)} + 2H_2O _ {(l)} \ rightarrow 2H_2SO_ {4 (aq)} \]
Какой объем of O 2 (в литрах) при 22 ° C и давлении 745 мм рт. ст. требуется для получения 1.00 тонн (907,18 кг) H 2 SO 4 ?
Дано: реакция, температура, давление и масса одного продукта
Запрошено: объем газообразного реагента
Стратегия:
A Рассчитать количество молей H 2 SO 4 в 1,00 тонне. Используя стехиометрические коэффициенты в сбалансированном химическом уравнении, рассчитайте необходимое количество молей O 2 .
B Используйте закон идеального газа, чтобы определить объем O 2 , необходимый в данных условиях.5 \; L \]
Ответ означает, что для производства 1 тонны серной кислоты необходимо более 300 000 л газообразного кислорода. Эти числа могут дать вам представление о масштабах инженерных и сантехнических проблем, с которыми сталкивается промышленная химия.
Упражнение 6.6.1
В примере 5 мы видели, что Чарльз использовал воздушный шар, содержащий приблизительно 31 150 л H 2 , для своего первого полета в 1783 году. Газообразный водород был получен реакцией металлического железа с разбавленной соляной кислотой. согласно следующему сбалансированному химическому уравнению:
\ [Fe _ {(s)} + 2 HCl _ {(aq)} \ rightarrow H_ {2 (g)} + FeCl_ {2 (aq)} \]
Сколько железа (в килограммах) требовалось для производства этого объема H 2 , если температура была 30 ° C, а атмосферное давление было 745 мм рт.
Ответ: 68.6 кг Fe (примерно 150 фунтов)
.