Какие химические свойства аммиака используют при получении продуктов
Помогите разобраться с рисунком Вопрос 10 § 15-18 Химия 9 класс Рудзитис, Фельдман
1—4, 8, 10, 11. Используется свойство аммиака
присоединять ион водорода по донорно-акцептор-
ному механизму. В результате образуются соли
аммония, которые и являются удобрениями.
5. NH4Cl используют при пайке металлов для
травления их поверхности. Он реагирует с окси-
дами металлов, образуя с ними летучие хлориды
и очищая таким образом поверхность спаиваемых
металлов от оксидов.
6. В медицине используется как местно-раздра-
жающее средство при невралгиях, укусах насе-
комых, в этом случае используется его основные
свойства, а так же при обморочных состояниях для
возбуждения дыхания — аммиак легко испаряется
из водного раствора и обладает резким запахом.
7. Аммиак хорошо растворяет жиры, поэтому
используется для стирки, удаления масляных пятен,
а также пятен молока, кофе.
9. Из смеси аммиачной селитры с различными
видами углеводородных горючих материалов полу-
чают взрывчатые вещества. При этом используются
очень сильные окислительные свойства азота в выс-
шей степени окисления +5.
12. Современный способ производства азотной
кислоты основан на каталитическом окислении син-
тетического аммиака на катализаторах до смеси ок-
сидов азота с дальнейшим поглощением их водой.
аммиака | Определение и использование
Аммиак (NH 3 ) , бесцветный едкий газ, состоящий из азота и водорода. Это простейшее стабильное соединение из этих элементов и служит исходным материалом для производства многих коммерчески важных соединений азота.
Аммиак и амины имеют слегка уплощенную треугольную пирамидальную форму с неподеленной парой электронов над азотом. В ионах четвертичного аммония эту область занимает четвертый заместитель.
Encyclopædia Britannica, Inc.Использование аммиака
Аммиак используется в основном в качестве удобрения. В США его обычно наносят непосредственно на почву из резервуаров, содержащих сжиженный газ. Аммиак также может быть в форме солей аммония, таких как нитрат аммония, NH 4 NO 3 , сульфат аммония (NH 4 ) 2 SO 4 и различные фосфаты аммония. Мочевина, (H 2 N) 2 C = O, является наиболее часто используемым источником азота для удобрений во всем мире.Аммиак также используется в производстве коммерческих взрывчатых веществ (например, тринитротолуола [TNT], нитроглицерина и нитроцеллюлозы).
В текстильной промышленности аммиак используется при производстве синтетических волокон, таких как нейлон и вискоза. Кроме того, он используется для окрашивания и чистки хлопка, шерсти и шелка. Аммиак служит катализатором при производстве некоторых синтетических смол. Что еще более важно, он нейтрализует кислотные побочные продукты нефтепереработки, а в резиновой промышленности предотвращает коагуляцию сырого латекса во время транспортировки с плантации на фабрику.Аммиак также находит применение как в аммиачно-содовом процессе (также называемом процессом Сольве), широко используемом методе производства кальцинированной соды, так и в процессе Оствальда, способе превращения аммиака в азотную кислоту.
Аммиак используется в различных металлургических процессах, включая азотирование листов сплава для упрочнения их поверхностей. Поскольку аммиак легко разлагается с образованием водорода, он является удобным портативным источником атомарного водорода для сварки. Кроме того, аммиак может поглощать значительное количество тепла из окружающей среды (т.е.е., один грамм аммиака поглощает 327 калорий тепла), что делает его полезным в качестве хладагента в холодильном оборудовании и оборудовании для кондиционирования воздуха. Наконец, среди его второстепенных применений - включение в некоторые бытовые чистящие средства.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняПолучение аммиака
Чистый аммиак был впервые получен английским ученым-физиком Джозефом Пристли в 1774 году, а его точный состав был определен французским химиком Клодом-Луи Бертолле в 1785 году.Аммиак неизменно входит в пятерку основных химических веществ, производимых в Соединенных Штатах. Основным промышленным методом производства аммиака является процесс Габера-Боша, который включает прямую реакцию элементарного водорода и элементарного азота. № 2 + 3H 2 → 2NH 3
Эта реакция требует использования катализатора, высокого давления (100–1000 атмосфер) и повышенной температуры (400–550 ° C [750–1020 ° F]). Фактически, равновесие между элементами и аммиаком способствует образованию аммиака при низкой температуре, но для достижения удовлетворительной скорости образования аммиака требуется высокая температура.Можно использовать несколько различных катализаторов. Обычно катализатор представляет собой железо, содержащее оксид железа. Однако как оксид магния на оксиде алюминия, который был активирован оксидами щелочных металлов, так и рутений на угле использовались в качестве катализаторов. В лаборатории аммиак лучше всего синтезировать путем гидролиза нитрида металла. Mg 3 N 2 + 6H 2 O → 2NH 3 + 3Mg (OH) 2
Физические свойства аммиака
Аммиак - бесцветный газ с резким резким запахом.Его точка кипения составляет -33,35 ° C (-28,03 ° F), а температура замерзания -77,7 ° C (-107,8 ° F). Он имеет высокую теплоту испарения (23,3 килоджоулей на моль при температуре кипения) и может обрабатываться как жидкость в теплоизолированных контейнерах в лаборатории. (Теплота испарения вещества - это количество килоджоулей, необходимое для испарения одного моля вещества без изменения температуры.) Молекула аммиака имеет треугольную пирамидальную форму с тремя атомами водорода и неподеленной парой электронов, прикрепленных к атом азота.Это полярная молекула, которая тесно связана из-за сильной межмолекулярной водородной связи. Диэлектрическая проницаемость аммиака (22 при -34 ° C [-29 ° F]) ниже, чем у воды (81 при 25 ° C [77 ° F]), поэтому он является лучшим растворителем для органических материалов. Однако он все еще достаточно высок, чтобы аммиак мог действовать как умеренно хороший ионизирующий растворитель. Аммиак также самоионизируется, хотя и в меньшей степени, чем вода. 2NH 3 ⇌ NH 4 + + NH 2 -
Химическая активность аммиака
Аммиак сгорает с трудом, но образует газообразный азот и воду.4NH 3 + 3O 2 + тепло → 2N 2 + 6H 2 O Однако при использовании катализатора и при правильных температурных условиях аммиак реагирует с кислородом с образованием оксида азота NO, который окисляется до диоксида азота NO 2 и используется в промышленном синтезе азотной кислоты.
Аммиак легко растворяется в воде с выделением тепла. NH 3 + H 2 O ⇌ NH 4 + + OH - Эти водные растворы аммиака являются основными и иногда их называют растворами гидроксида аммония (NH 4 OH).Равновесие, однако, таково, что 1,0-молярный раствор NH 3 дает только 4,2 миллимоля гидроксид-иона. Гидраты NH 3 · H 2 O, 2NH 3 · H 2 O и NH 3 · 2H 2 O существуют и, как было показано, состоят из молекул аммиака и воды, связанных межмолекулярной связью. водородные связи.
Аммиак жидкий широко используется в качестве неводного растворителя. Щелочные металлы, а также более тяжелые щелочноземельные металлы и даже некоторые внутренние переходные металлы растворяются в жидком аммиаке, образуя синие растворы.Физические измерения, в том числе исследования электропроводности, свидетельствуют о том, что этот синий цвет и электрический ток связаны с сольватированным электроном. металл (рассеянный) ⇌ металл (NH 3 ) x ⇌ M + (NH 3 ) x + e - (NH 3 ) y Эти растворы являются отличными источниками электронов для восстановления других химических соединений. По мере увеличения концентрации растворенного металла раствор становится более глубокого синего цвета и, наконец, превращается в раствор цвета меди с металлическим блеском.Электропроводность уменьшается, и есть свидетельства того, что сольватированные электроны объединяются с образованием электронных пар. 2 e - (NH 3 ) y ⇌ e 2 (NH 3 ) y Большинство солей аммония также легко растворяются в жидком аммиаке.
.Физические свойства аминов с характеристиками и классификацией
-
- БЕСПЛАТНАЯ ЗАПИСЬ КЛАСС
- КОНКУРСНЫЕ ЭКЗАМЕНА
- BNAT
- Классы
- Класс 1-3
- Класс 4-5
- Класс 6-10
- Класс 110003 CBSE
- Книги NCERT
- Книги NCERT для класса 5
- Книги NCERT, класс 6
- Книги NCERT для класса 7
- Книги NCERT для класса 8
- Книги NCERT для класса 9
- Книги NCERT для класса 10
- NCERT Книги для класса 11
- NCERT Книги для класса 12
- NCERT Exemplar
- NCERT Exemplar Class 8
- NCERT Exemplar Class 9
- NCERT Exemplar Class 10
- NCERT Exemplar Class 11 9plar
- RS Aggarwal
- RS Aggarwal Решения класса 12
- RS Aggarwal Class 11 Solutions
- RS Aggarwal Решения класса 10
- Решения RS Aggarwal класса 9
- Решения RS Aggarwal класса 8
- Решения RS Aggarwal класса 7
- Решения RS Aggarwal класса 6
- RD Sharma
- RD Sharma Class 6 Решения
- RD Sharma Class 7 Решения
- Решения RD Sharma Class 8
- Решения RD Sharma Class 9
- Решения RD Sharma Class 10
- Решения RD Sharma Class 11
- Решения RD Sharma Class 12
- PHYSICS
- Механика
- Оптика
- Термодинамика
- Электромагнетизм
- ХИМИЯ
- Органическая химия
- Неорганическая химия
- Периодическая таблица
- MATHS
- Статистика
- Числа
- Числа Пифагора Тр Игонометрические функции
- Взаимосвязи и функции
- Последовательности и серии
- Таблицы умножения
- Детерминанты и матрицы
- Прибыль и убыток
- Полиномиальные уравнения
- Разделение фракций
- Microology
- Книги NCERT
- FORMULAS
- Математические формулы
- Алгебраные формулы
- Тригонометрические формулы
- Геометрические формулы
- КАЛЬКУЛЯТОРЫ
- Математические калькуляторы 0003000
- 000
- 000 Калькуляторы по химии
- 000
- 000
- 000 Образцы документов для класса 6
- Образцы документов CBSE для класса 7
- Образцы документов CBSE для класса 8
- Образцы документов CBSE для класса 9
- Образцы документов CBSE для класса 10
- Образцы документов CBSE для класса 1 1
- Образцы документов CBSE для класса 12
- Вопросники предыдущего года CBSE
- Вопросники предыдущего года CBSE, класс 10
- Вопросники предыдущего года CBSE, класс 12
- HC Verma Solutions
- HC Verma Solutions Класс 11 Физика
- Решения HC Verma Физика класса 12
- Решения Лакмира Сингха
- Решения Лакмира Сингха класса 9
- Решения Лахмира Сингха класса 10
- Решения Лакмира Сингха класса 8
9000 Класс
- Дополнительные вопросы по математике класса 8 CBSE
- Дополнительные вопросы по науке 8 класса CBSE
- Дополнительные вопросы по математике класса 9 CBSE
- Дополнительные вопросы по науке
- CBSE Вопросы
- CBSE Class 10 Дополнительные вопросы по математике
- CBSE Class 10 Science Extra questions
- Class 3
- Class 4
- Class 5
- Class 6
- Class 7
- Class 8 Класс 9
- Класс 10
- Класс 11
- Класс 12
- Решения NCERT для класса 11
- Решения NCERT для класса 11 по физике
- Решения NCERT для класса 11 Химия
- Решения NCERT для биологии класса 11
- Решение NCERT s Для класса 11 по математике
- NCERT Solutions Class 11 Accountancy
- NCERT Solutions Class 11 Business Studies
- NCERT Solutions Class 11 Economics
- NCERT Solutions Class 11 Statistics
- NCERT Solutions Class 11 Commerce
- NCERT Solutions for Class 12
- Решения NCERT для физики класса 12
- Решения NCERT для химии класса 12
- Решения NCERT для биологии класса 12
- Решения NCERT для математики класса 12
- Решения NCERT, класс 12, бухгалтерия
- Решения NCERT, класс 12, бизнес-исследования
- NCERT Solutions Class 12 Economics
- NCERT Solutions Class 12 Accountancy Part 1
- NCERT Solutions Class 12 Accountancy Part 2
- NCERT Solutions Class 12 Micro-Economics
- NCERT Solutions Class 12 Commerce
- NCERT Solutions Class 12 Macro-Economics
- NCERT Solut Ионы Для класса 4
- Решения NCERT для математики класса 4
- Решения NCERT для класса 4 EVS
- Решения NCERT для класса 5
- Решения NCERT для математики класса 5
- Решения NCERT для класса 5 EVS
- Решения NCERT для класса 6
- Решения NCERT для математики класса 6
- Решения NCERT для науки класса 6
- Решения NCERT для класса 6 по социальным наукам
- Решения NCERT для класса 6 Английский язык
- Решения NCERT для класса 7
- Решения NCERT для математики класса 7
- Решения NCERT для науки класса 7
- Решения NCERT для социальных наук класса 7
- Решения NCERT для класса 7 Английский язык
- Решения NCERT для класса 8
- Решения NCERT для математики класса 8
- Решения NCERT для науки 8 класса
- Решения NCERT для социальных наук 8 класса ce
- Решения NCERT для класса 8 Английский
- Решения NCERT для класса 9
- Решения NCERT для класса 9 по социальным наукам
- Решения NCERT для математики класса 9
- Решения NCERT для математики класса 9 Глава 1
- Решения NCERT для математики класса 9, глава 2 Решения NCERT
- для математики класса 9, глава 3
- Решения NCERT для математики класса 9, глава 4
- Решения NCERT для математики класса 9, глава 5 Решения NCERT
- для математики класса 9, глава 6
- Решения NCERT для математики класса 9 Глава 7 Решения NCERT
- для математики класса 9 Глава 8
- Решения NCERT для математики класса 9 Глава 9
- Решения NCERT для математики класса 9 Глава 10 Решения NCERT
- для математики класса 9 Глава 11 Решения
- NCERT для математики класса 9 Глава 12 Решения NCERT
- для математики класса 9 Глава 13
- NCER Решения T для математики класса 9 Глава 14
- Решения NCERT для математики класса 9 Глава 15
- Решения NCERT для науки класса 9
- Решения NCERT для науки класса 9 Глава 1
- Решения NCERT для науки класса 9 Глава 2
- Решения NCERT для науки класса 9 Глава 3
- Решения NCERT для науки класса 9 Глава 4
- Решения NCERT для науки класса 9 Глава 5
- Решения NCERT для науки класса 9 Глава 6
- Решения NCERT для науки класса 9 Глава 7
- Решения NCERT для науки класса 9 Глава 8
- Решения NCERT для науки класса 9 Глава 9
- Решения NCERT для науки класса 9 Глава 10
- Решения NCERT для науки класса 9 Глава 12
- Решения NCERT для науки класса 9 Глава 11
- Решения NCERT для науки класса 9 Глава 13 Решения NCERT
- для науки класса 9 Глава 14
- Решения NCERT для класса 9 по науке Глава 15
- Решения NCERT для класса 10
- Решения NCERT для класса 10 по социальным наукам
- Решения NCERT для математики класса 10
- Решения NCERT для математики класса 10 Глава 1
- Решения NCERT для математики класса 10, глава 2
- Решения NCERT для математики класса 10, глава 3
- Решения NCERT для математики класса 10, глава 4
- Решения NCERT для математики класса 10, глава 5 Решения NCERT для математики класса 10, глава 6
- Решения NCERT для математики класса 10, глава 7
- Решения NCERT для математики класса 10, глава 8
- Решения NCERT для математики класса 10, глава 9
- Решения NCERT для математики класса 10, глава 10
- Решения NCERT для математики класса 10 Глава 11
- Решения NCERT для математики класса 10 Глава 12
- Решения NCERT для математики класса 10 Глава ter 13
- Решения NCERT для математики класса 10, глава 14
- Решения NCERT для математики класса 10, глава 15
- Решения NCERT для класса 10, наука, глава 1
- Решения NCERT для класса 10 Наука, глава 2
- Решения NCERT для класса 10, глава 3
- Решения NCERT для класса 10, глава 4
- Решения NCERT для класса 10, глава 5
- Решения NCERT для класса 10, глава 6
- Решения NCERT для класса 10 Наука, глава 7
- Решения NCERT для класса 10, глава 8,
- Решения NCERT для класса 10, глава 9
- Решения NCERT для класса 10, глава 10
- Решения NCERT для класса 10, глава 11
- Решения NCERT для класса 10 Наука Глава 12
- Решения NCERT для класса 10 Наука Глава 13
- NCERT S Решения для класса 10 по науке Глава 14
- Решения NCERT для класса 10 по науке Глава 15
- Решения NCERT для класса 10 по науке Глава 16
- Class 11 Commerce Syllabus
- Учебный план класса 11
- Учебный план класса 11
- Учебный план экономического факультета 11
- Учебный план по коммерции класса 12
- Учебный план класса 12
- Учебный план класса 12
- Учебный план
- Класс 12 Образцы документов для коммерции
- Образцы документов для коммерции класса 11
- Образцы документов для коммерции класса 12
- TS Grewal Solutions
- TS Grewal Solutions Class 12 Accountancy
- TS Grewal Solutions Class 11 Accountancy
- Отчет о движении денежных средств 9 0004
- Что такое предпринимательство
- Защита прав потребителей
- Что такое основные средства
- Что такое баланс
- Что такое фискальный дефицит
- Что такое акции
- Разница между продажами и маркетингом
- ICC
- Образцы документов ICSE
- Вопросы ICSE
- ML Aggarwal Solutions
- ML Aggarwal Solutions Class 10 Maths
- ML Aggarwal Solutions Class 9 Maths
- ML Aggarwal Solutions Class 8 Maths
- ML Aggarwal Solutions Class 7 Maths Решения Математика класса 6
- Решения Селины
- Решения Селины для класса 8
- Решения Селины для класса 10
- Решение Селины для класса 9
- Решения Фрэнка
- Решения Фрэнка для математики класса 10
- Франк Решения для математики 9 класса
- ICSE Class
- ICSE Class 6
- ICSE Class 7
- ICSE Class 8
- ICSE Class 9
- ICSE Class 10
- ISC Class 11
- ISC Class 12
- 900 Экзамен IAS
- Пробный тест IAS 2019 1
- Пробный тест IAS4
- Экзамен KPSC KAS
- Экзамен UPPSC PCS
- Экзамен MPSC
- Экзамен RPSC RAS
- TNPSC Group 1
- APPSC Group 1
- Экзамен BPSC
- Экзамен WPSC
- Экзамен JPSC
- Экзамен GPSC
- Ответный ключ UPSC 2019
- Коучинг IAS Бангалор
- Коучинг IAS Дели
- Коучинг IAS Ченнаи
- Коучинг IAS Хайдарабад
- Коучинг IAS Мумбаи
- Программа BYJU NEET
- NEET 2020
- NEET Eligibility
- NEET Eligibility
- NEET Eligibility 2020 Подготовка
- NEET Syllabus
- Support
- Разрешение жалоб
- Служба поддержки
- Центр поддержки
- GSEB
- GSEB Syllabus
- GSEB Образец
- MSBSHSE Syllabus
- MSBSHSE Учебники
- MSBSHSE Образцы статей
- MSBSHSE Вопросы
- 9000
- AP 2 Year Syllabus
- MP Board Syllabus
- MP Board Образцы документов
- Учебники MP Board
- Assam Board Syllabus
- Assam Board
- Assam Board
- Assam Board Документы
- Bihar Board Syllabus
- Bihar Board Учебники
- Bihar Board Question Papers
- Bihar Board Model Papers
- Odisha Board
- Odisha Board
- Odisha Board 9000
- ПСЕБ 9 0002
- PSEB Syllabus
- PSEB Учебники
- PSEB Вопросы и ответы
- RBSE
- Rajasthan Board Syllabus
- RBSE Учебники
- RBSE
- 000 RBSE 000 HPOSE
- 000 HPOSE
- 000 000 HPOSE
- 000 HPOSE
- 000 000
000 HPOSE - 000 HPOSE 000
- JKBOSE Syllabus
- JKBOSE Образцы документов
- Экзамен JKBOSE P
метана | Определение, свойства, использование и факты
Метан , бесцветный газ без запаха, который часто встречается в природе и является продуктом определенной деятельности человека. Метан - простейший член парафинового ряда углеводородов и один из самых сильных парниковых газов. Его химическая формула - CH 4 .
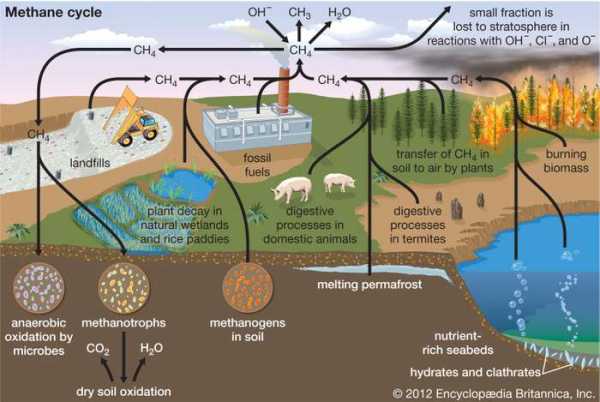 метановый цикл Encyclopdia Britannica, Inc.
метановый цикл Encyclopdia Britannica, Inc. 
Британская викторина
Ветер и воздух: факт или вымысел?
Муссонные ветры встречаются в нескольких регионах мира.
Химические свойства метана
Метан легче воздуха, его удельный вес составляет 0,554. Он слабо растворяется в воде. Легко горит на воздухе, образуя углекислый газ и водяной пар; пламя бледное, слегка яркое и очень горячее. Точка кипения метана составляет -162 ° C (-259,6 ° F), а точка плавления -182,5 ° C (-296,5 ° F). Метан в целом очень стабилен, но смеси метана и воздуха с содержанием метана от 5 до 14 процентов по объему взрывоопасны.Взрывы таких смесей часто случаются на угольных шахтах и угольных шахтах и являются причиной многих аварий на шахтах.
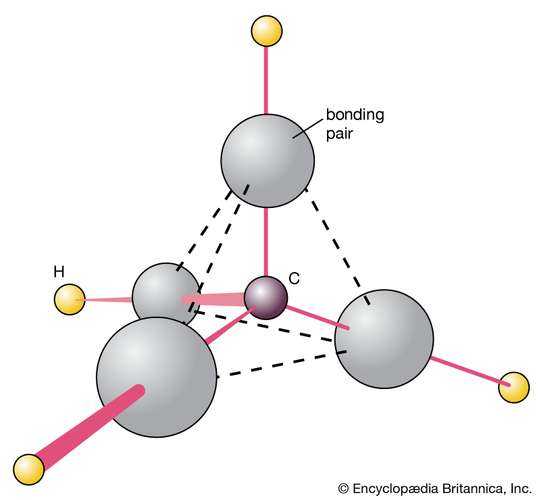 структура метана
структура метана Тетраэдрическая структура метана (CH 4 ) объясняется в теории VSEPR (валентная оболочка-электронная пара отталкивания) молекулярной формы, предполагая, что четыре пары связывающих электронов (представленные серые облака) занимают позиции, минимизирующие их взаимное отталкивание.
Encyclopædia Britannica, Inc.Источники метана
В природе метан образуется в результате анаэробного бактериального разложения растительных веществ под водой (где его иногда называют болотным газом или болотным газом). Водно-болотные угодья являются основным естественным источником производимого таким образом метана. Другие важные природные источники метана включают термитов (в результате процессов пищеварения), вулканы, жерла на дне океана и отложения гидрата метана, которые встречаются вдоль окраин континентов и под антарктическими льдами и арктической вечной мерзлотой.Метан также является основным компонентом природного газа, который содержит от 50 до 90 процентов метана (в зависимости от источника) и встречается как компонент горючего газа (горючего газа) вдоль угольных пластов.
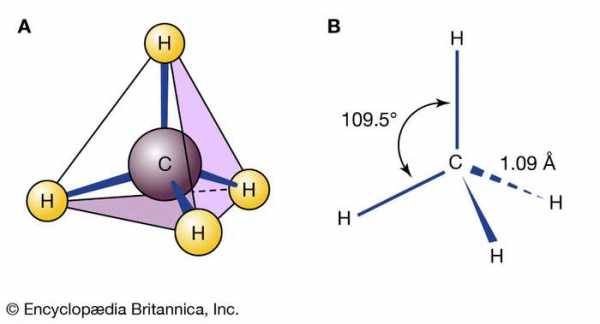 химическая структура метана
химическая структура метана Тетраэдрическая геометрия метана: (A) модель стержня и шарика и (B) диаграмма, показывающая валентные углы и расстояния. (Простые связи обозначают связи в плоскости изображения; клин и пунктирные связи обозначают связи, направленные к зрителю и от него, соответственно.)
Encyclopædia Britannica, Inc.Производство и сжигание природного газа и угля являются основными антропогенными (связанными с деятельностью человека) источниками метана. Такие виды деятельности, как добыча и обработка природного газа и деструктивная перегонка битуминозного угля при производстве угольного и коксового газа, приводят к выбросу значительных количеств метана в атмосферу. Другая деятельность человека, связанная с производством метана, включает сжигание биомассы, животноводство и управление отходами (где бактерии производят метан, разлагая отстой в очистных сооружениях и разлагающийся материал на свалках).
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняИспользование метана
Метан - важный источник водорода и некоторых органических химикатов. Метан реагирует с паром при высоких температурах с образованием окиси углерода и водорода; последний используется при производстве аммиака для удобрений и взрывчатых веществ. Другие ценные химические вещества, полученные из метана, включают метанол, хлороформ, четыреххлористый углерод и нитрометан. При неполном сгорании метана образуется технический углерод, который широко используется в качестве армирующего агента в резине, используемой для автомобильных шин.
Роль как парниковый газ
Метан, который производится и выбрасывается в атмосферу, поглощается стоками метана, которые включают почву и процесс окисления метана в тропосфере (нижний уровень атмосферы). Большая часть метана, производимого естественным путем, компенсируется его поглощением в естественных стоках. Однако антропогенное производство метана может вызвать более быстрое увеличение концентраций метана, чем они компенсируются поглотителями. С 2007 года концентрация метана в атмосфере Земли увеличилась в 6 раз.8–10 частей на миллиард (ppb) в год. К 2020 году содержание метана в атмосфере достигло 1873,5 частей на миллиард, что примерно в два-три раза выше, чем доиндустриальные уровни, которые колебались на уровне 600-700 частей на миллиард.
Повышенная концентрация метана в атмосфере способствует парниковому эффекту, в результате чего парниковые газы (особенно углекислый газ, метан и водяной пар) поглощают инфракрасное излучение (чистую тепловую энергию) и повторно излучают его обратно на поверхность Земли, потенциально задерживая тепло и производя существенные изменения климата.Повышенное содержание метана в атмосфере также косвенно увеличивает парниковый эффект. Например, при окислении метана гидроксильные радикалы (OH -) удаляют метан, вступая в реакцию с ним с образованием диоксида углерода и водяного пара, а по мере увеличения концентрации атмосферного метана концентрация гидроксильных радикалов уменьшается, что эффективно продлевает срок службы метана в атмосфере. .
The Editors of Encyclopaedia Britannica Эта статья была недавно отредактирована и обновлена редактором Джоном П. Рафферти.Узнайте больше в этих связанных статьях Britannica:
-
глобальное потепление: метан
Метан (CH 4 ) - второй по значимости парниковый газ. CH 4 более мощный, чем CO 2 , потому что радиационное воздействие, производимое на одну молекулу, больше.Кроме того, инфракрасное окно менее насыщено в диапазоне длин волн излучения, поглощаемого CH 4 , поэтому больше…
-
парниковый газ: метан
Метан (CH 4 ) - второй по значимости парниковый газ.CH 4 более мощный, чем CO 2 , потому что радиационное воздействие, производимое на одну молекулу, больше. Кроме того, инфракрасное окно менее насыщено в диапазоне длин волн излучения, поглощаемого CH 4 , поэтому больше…
-
Климат: Климат и жизнь
… пар, двуокись углерода, окись углерода, метан, озон, двуокись азота, азотная кислота, аммиак и ионы аммония, закись азота, двуокись серы, сероводород, карбонилсульфид, диметилсульфид и сложный набор неметановых углеводородов.Из них…
химическое соединение | Определение, примеры и типы
Химическое соединение , любое вещество, состоящее из идентичных молекул, состоящих из атомов двух или более химических элементов.
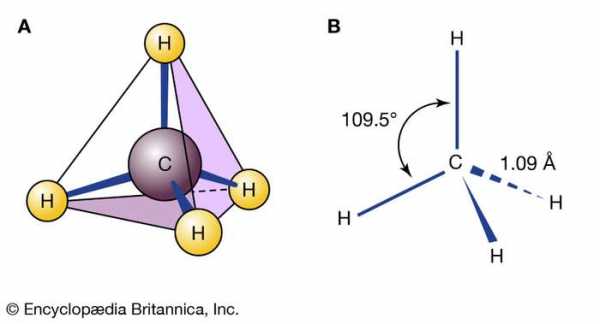 молекула метана
молекула метана Метан, в котором четыре атома водорода связаны с одним атомом углерода, является примером основного химического соединения. На структуру химических соединений влияют сложные факторы, такие как валентные углы и длина связи.
Encyclopædia Britannica, Inc.
Британская викторина
Подводки к химии
Какой электрический заряд у электрона?
Вся материя Вселенной состоит из атомов более чем 100 различных химических элементов, которые встречаются как в чистом виде, так и в сочетании в химических соединениях.Образец любого данного чистого элемента состоит только из атомов, характерных для этого элемента, и атомы каждого элемента уникальны. Например, атомы углерода отличаются от атомов железа, которые, в свою очередь, отличаются от атомов золота. Каждый элемент обозначается уникальным символом, состоящим из одной, двух или трех букв, возникающих либо из текущего имени элемента, либо из его исходного (часто латинского) имени. Например, символы углерода, водорода и кислорода - это просто C, H и O соответственно.Символ железа - Fe, от оригинального латинского названия ferrum . Фундаментальный принцип химической науки состоит в том, что атомы различных элементов могут объединяться друг с другом с образованием химических соединений. Например, метан, который образован из элементов углерода и водорода в соотношении четыре атома водорода на каждый атом углерода, как известно, содержит отдельные молекулы CH 4 . Формула соединения - например, CH 4 - указывает типы присутствующих атомов, с нижними индексами, представляющими относительное количество атомов (хотя цифра 1 никогда не записывается).
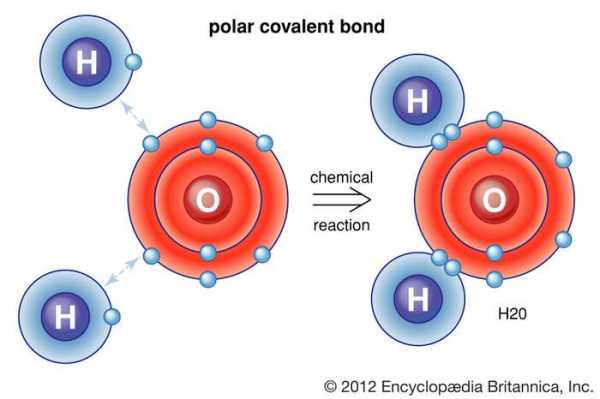 молекула воды
молекула воды Молекула воды состоит из двух атомов водорода и одного атома кислорода. Один атом кислорода содержит шесть электронов в своей внешней оболочке, которая может содержать в общей сложности восемь электронов. Когда два атома водорода связаны с атомом кислорода, внешняя электронная оболочка кислорода заполняется.
Encyclopædia Britannica, Inc.-
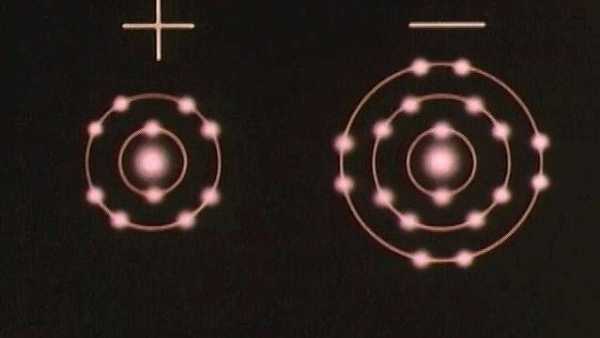 Исследуйте магнитоподобную ионную связь, образующуюся при передаче электронов от одного атома к другому
Исследуйте магнитоподобную ионную связь, образующуюся при передаче электронов от одного атома к другому Ионы - атомы с положительным или отрицательным суммарным зарядом - связываются вместе, образуя ионные соединения.
Encyclopædia Britannica, Inc. См. Все видео для этой статьи -
 Посмотрите, как работают молекулярные связи, когда два атома водорода присоединяются к атому серы, образуя сероводород
Посмотрите, как работают молекулярные связи, когда два атома водорода присоединяются к атому серы, образуя сероводород Молекулярные соединения образуются, когда молекулы, такие как молекулы метана или вода, соединяются вместе, разделяя электроны.
Encyclopædia Britannica, Inc. Посмотреть все видео по этой статье
Вода, которая представляет собой химическое соединение водорода и кислорода в соотношении два атома водорода на каждый атом кислорода, содержит молекулы H 2 O.Хлорид натрия - это химическое соединение, образованное из натрия (Na) и хлора (Cl) в соотношении 1: 1. Хотя формула хлорида натрия - NaCl, соединение не содержит реальных молекул NaCl. Скорее, он содержит равное количество ионов натрия с положительным зарядом (Na + ) и ионов хлора с отрицательным зарядом (Cl - ). ( См. Ниже Тенденции в химических свойствах элементов для обсуждения процесса превращения незаряженных атомов в ионы [i.е., виды с положительным или отрицательным суммарным зарядом].) Упомянутые выше вещества представляют два основных типа химических соединений: молекулярные (ковалентные) и ионные. Метан и вода состоят из молекул; то есть они являются молекулярными соединениями. С другой стороны, хлорид натрия содержит ионы; это ионное соединение.
Атомы различных химических элементов можно сравнить с буквами алфавита: так же, как буквы алфавита объединяются, образуя тысячи слов, атомы элементов могут объединяться различными способами, образуя бесчисленное множество соединений. .На самом деле известны миллионы химических соединений, и многие миллионы возможны, но еще не открыты или синтезированы. Большинство веществ, встречающихся в природе, таких как древесина, почва и камни, представляют собой смеси химических соединений. Эти вещества могут быть разделены на составляющие их соединения физическими методами, которые не изменяют способ агрегирования атомов в соединениях. Соединения можно разделить на составные элементы путем химических изменений.Химическое изменение (то есть химическая реакция) - это изменение, при котором организация атомов изменяется. Примером химической реакции является горение метана в присутствии молекулярного кислорода (O 2 ) с образованием диоксида углерода (CO 2 ) и воды. CH 4 + 2O 2 → CO 2 + 2H 2 O В этой реакции, которая является примером реакции горения, происходят изменения в том, как атомы углерода, водорода и кислорода связаны друг с другом. в соединениях.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняХимические соединения обладают поразительным набором характеристик. При обычных температурах и давлениях некоторые из них являются твердыми телами, некоторые - жидкостями, а некоторые - газами. Цвета различных составных частей совпадают с цветами радуги. Некоторые соединения очень токсичны для человека, тогда как другие необходимы для жизни. Замена только одного атома в соединении может быть причиной изменения цвета, запаха или токсичности вещества.Чтобы понять это огромное разнообразие, были разработаны системы классификации. В приведенном выше примере соединения классифицируются как молекулярные или ионные. Соединения также подразделяются на органические и неорганические. Органические соединения ( см. Ниже Органические соединения), названные так потому, что многие из них были первоначально изолированы от живых организмов, обычно содержат цепи или кольца атомов углерода. Из-за огромного разнообразия способов связывания углерода и других элементов существует более девяти миллионов органических соединений.Соединения, которые не считаются органическими, называются неорганическими соединениями ( см. Ниже Неорганические соединения).
 ртуть (Hg)
ртуть (Hg) Ртуть (химический символ: Hg) - единственный металлический элемент, который является жидким при комнатной температуре.
© marcel / FotoliaВ рамках широкой классификации органических и неорганических веществ существует множество подклассов, в основном основанных на конкретных элементах или группах присутствующих элементов. Например, среди неорганических соединений оксиды содержат ионы O 2- или атомы кислорода, гидриды содержат ионы H - или атомы водорода, сульфиды содержат ионы S 2- и т. Д.Подклассы органических соединений включают спирты (содержащие группу OH), карбоновые кислоты (характеризующиеся группой COOH), амины (содержащие группу NH 2 ) и так далее.
Различные способности различных атомов объединяться с образованием соединений лучше всего можно понять с помощью периодической таблицы. Периодическая таблица Менделеева была первоначально построена для представления закономерностей, наблюдаемых в химических свойствах элементов ( см. химическая связь). Другими словами, по мере развития науки химии было замечено, что элементы можно сгруппировать в соответствии с их химической реакционной способностью.Элементы с подобными свойствами перечислены в вертикальных столбцах периодической таблицы и называются группами. По мере раскрытия деталей атомной структуры стало ясно, что положение элемента в периодической таблице коррелирует с расположением электронов, которыми обладают атомы этого элемента ( см. Атом ). В частности, было замечено, что электроны, которые определяют химическое поведение атома, находятся в его внешней оболочке. Такие электроны называются валентными электронами.
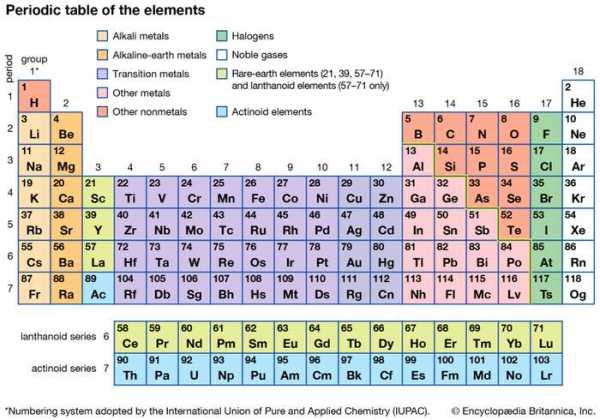 таблица Менделеева
таблица Менделеева Периодическая таблица элементов.
Encyclopædia Britannica, Inc.Например, атомы элементов в группе 1 периодической таблицы все имеют один валентный электрон, атомы элементов в группе 2 имеют два валентных электрона, и так далее, до группы 18 , элементы которого содержат восемь валентных электронов. Самое простое и самое важное правило для предсказания того, как атомы образуют соединения, заключается в том, что атомы имеют тенденцию объединяться таким образом, чтобы они могли либо опустошить свою валентную оболочку, либо завершить ее (т.е., заполните его), в большинстве случаев всего с восемью электронами. Элементы в левой части таблицы Менделеева имеют тенденцию терять свои валентные электроны в химических реакциях. Натрий (в Группе 1), например, имеет тенденцию терять свой одинокий валентный электрон с образованием иона с зарядом +1. Каждый атом натрия имеет 11 электронов ( e - ), каждый с зарядом -1, чтобы просто сбалансировать заряд +11 на его ядре. Потеря одного электрона оставляет у него 10 отрицательных зарядов и 11 положительных зарядов, что дает суммарный заряд +1: Na → Na + + e -.Калий, расположенный непосредственно под натрием в Группе 1, также образует в своих реакциях +1 ион (K + ), как и остальные члены Группы 1: рубидий (Rb), цезий (Cs) и франций (Fr). Атомы элементов в правом конце периодической таблицы имеют тенденцию вступать в реакции, так что они получают (или разделяют) достаточно электронов, чтобы заполнить свою валентную оболочку. Например, кислород в группе 16 имеет шесть валентных электронов и, следовательно, нуждается в двух дополнительных электронах для завершения своей внешней оболочки. Кислород достигает этого за счет реакции с элементами, которые могут терять или делиться электронами.Атом кислорода, например, может реагировать с атомом магния (Mg) (в Группе 2), принимая два валентных электрона магния, образуя ионы Mg 2+ и O 2−. (Когда нейтральный атом магния теряет два электрона, он образует ион Mg 2+ , а когда нейтральный атом кислорода получает два электрона, он образует ион O 2-.) Получающийся в результате Mg 2+ и O 2- затем объединяют в соотношении 1: 1 с получением ионного соединения MgO (оксид магния). (Хотя составной оксид магния содержит заряженные частицы, у него нет чистого заряда, поскольку он содержит равное количество ионов Mg 2+ и O 2-.) Аналогичным образом кислород реагирует с кальцием (чуть ниже магния в группе 2) с образованием CaO (оксид кальция). Кислород аналогичным образом реагирует с бериллием (Be), стронцием (Sr), барием (Ba) и радием (Ra), остальными элементами группы 2. Ключевым моментом является то, что, поскольку все элементы в данной группе имеют одинаковое количество валентных электронов, они образуют аналогичные соединения.
Химические элементы можно классифицировать по-разному. Наиболее фундаментальное разделение элементов - на металлы, которые составляют большинство элементов, и неметаллы.Типичные физические свойства металлов - это блестящий внешний вид, пластичность (способность растираться в тонкий лист), пластичность (способность вытягиваться в проволоку), а также эффективная тепло- и электропроводность. Самым важным химическим свойством металлов является тенденция отдавать электроны с образованием положительных ионов. Например, медь (Cu) - типичный металл. Он блестящий, но легко тускнеет; это отличный проводник электричества и обычно используется для электрических проводов; и из него легко превращаться в изделия различной формы, такие как трубы для систем водоснабжения.Медь содержится во многих ионных соединениях в форме иона Cu + или Cu 2+ .
Металлические элементы находятся на левой стороне и в центре таблицы Менделеева. Металлы групп 1 и 2 называются типичными металлами; те, что находятся в центре периодической таблицы, называются переходными металлами. Лантаноиды и актиноиды, показанные под периодической таблицей, представляют собой особые классы переходных металлов.
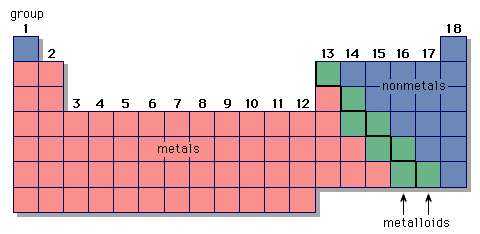 металлических элементов в периодической таблице Менделеева
металлических элементов в периодической таблице Менделеева Металлы, неметаллы и металлоиды представлены в различных частях периодической таблицы Менделеева.
Encyclopædia Britannica, Inc.Неметаллы, которых относительно мало, находятся в верхнем правом углу таблицы Менделеева, за исключением водорода, единственного неметаллического члена группы 1. Физические свойства, характерные для металлы в неметаллах отсутствуют. В химических реакциях с металлами неметаллы приобретают электроны с образованием отрицательных ионов. Неметаллические элементы также реагируют с другими неметаллами, в этом случае образуя молекулярные соединения. Хлор - типичный неметалл.При обычных температурах элементарный хлор содержит молекулы Cl 2 и реагирует с другими неметаллами с образованием таких молекул, как HCl, CCl 4 и PCl 3 . Хлор реагирует с металлами с образованием ионных соединений, содержащих ионы Cl - .
Разделение элементов на металлы и неметаллы является приблизительным. Некоторые элементы вдоль разделительной линии проявляют как металлические, так и неметаллические свойства и называются металлоидами или полуметаллами.
.









