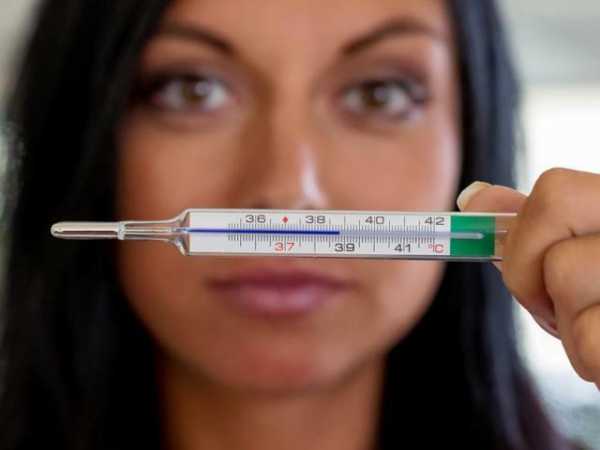
В каких продуктах есть азот
где его больше всего, список продуктов питания, богатых данным элементом
Азот входит в состав земной атмосферы в молекулярном виде, на него приходится 76% атмосферы по массе.
В связанном состоянии элемент встречается в почве и воде в виде химических соединений.
В живых организмах (растениях и животных) азот представлен в составе органических соединений, входит в аминокислоты в количестве от 15% до 18%.
к оглавлению ↑Как влияет на организм
В начале 20 века было установлено, что для обеспечения жизнедеятельности живых организмов необходимо регулярное поступление в них некоторых химических соединений, включая азот.

В теле мужчины содержится в среднем 1,8 кг элемента, а женщины – 1,3 кг. Такая разница обусловлена тем, что белки входят в состав мышечной ткани, а у мужчин мышцы развиты сильнее, чем у женщин.
Для человека атмосферный азот является биологически неактивным веществом, поступающим в легкие с вдыхаемым воздухом и выводимым с выдыхаемым.
Потребность человека в белке складывается из 2 компонентов – удовлетворение потребности в общем азоте и в незаменимых аминокислотах.
Белковые соединения для синтеза своих тканей человек получает из пищи, которая должна содержать достаточное их количество.
Из необходимых организму аминокислот некоторые (называемые заменимыми) синтезируются в организме из аммиака и иных веществ, а несинтезируемые (называемые незаменимыми) должны поступать с пищей (растительной и животной).
Чтобы атмосферный азот оказался в составе белков, он должен претерпеть ряд превращений. Использовать его напрямую способны лишь живущие в почве бактерии рода Азотобактер с дальнейшим синтезом органических азотистых соединений.
Все остальные живые организмы не способны использовать атмосферный азот. У них азотистый обмен начинается с использования аммиака или аминокислот.
Аммиак образуют высшие растения путем восстановления содержащихся в почве нитратов с конечным биосинтезом аминокислот и белков.
Травоядные животные питаются растениями и превращают аминокислоты растений в собственные белки. Человек потребляет растительные и животные продукты и также превращает их в собственные ткани.
После смерти живых организмов микроорганизмы расщепляют органические вещества, азот поступает в почву, где ассимилируется азотфиксирующими бактериями и вновь превращается в органические вещества. Это и есть кругооборот азота в природе.
к оглавлению ↑Потребность человека в белке, симптомы дефицита
В конце 19 века было окончательно установлено, что при нормальных условиях организм человека находится в состоянии азотистого равновесия, т. е. поступление азота с пищей равняется количеству элемента в выделяемых с мочой азотистых веществах (мочевине).

Количество выделяемой взрослым человеком мочевины зависит от количества потребляемой белковой пищи и обычно составляет 25-35 г в сутки.
Азотистый баланс нарушается при голодании или недостатке в пище белков. Длительное состояние отрицательного азотистого баланса (когда азота выводится больше, чем поступает) ведет к гибели организма.
Положительный азотистый баланс наблюдается в период восстановления после голодания или истощения. Нормальным является положительный азотистый баланс у растущих детей и подростков до периода прекращения их роста.
Для поддержания азотистого равновесия человеку, по нормам Всемирной организации здравоохранения, достаточно потреблять ежесуточно 0,8 г полноценного по аминокислотному составу белка на каждый килограмм своего веса.
При смешанном растительно-животном питании потребность в связи со снижением усвояемости возрастает и доходит до 1,0 г/кг. Под весом при данном расчете понимается нормальный (идеальный) вес без учета избыточной жировой ткани, например, по формуле «Рост минус 105».
При перечисленных ниже состояниях потребность в белке (и в азоте) увеличивается:
- стрессы;
- заболевания и травмы;
- после хирургических операций;
- беременность;
- грудное вскармливание;
- интенсивная физическая нагрузка.

При избыточном весе и похудении на сниженном по калорийности рационе также необходимо увеличить норму белка до 1,2-1,3 г/кг.
Но здесь нужна мера – потребление белка в количестве свыше 1,5 г/кг нежелательно, а свыше 2 г/кг — вредно.
Рекомендации по потреблению больших доз отдельных аминокислот или их комбинаций в виде добавки для спортсменов силовых видов спорта и бодибилдеров не подтверждаются, а применение чистых аминокислот считается неблагоприятным для здоровья, тем более, если они поступают взамен белковой пищи.
В чистом виде белковая недостаточность встречается редко. Это следствие общего недоедания, т. е. недостаточности калорийности рациона. Состояние при одновременном глубоком дефиците белка и энергии называется маразмом.
К социальным причинам недостаточности питания относятся:
- стихийные бедствия;
- войны;
- терроризм.
Поражает белково-энергетическая недостаточность беднейшие слои населения.
В развитых странах белково-калорийная недостаточность может наступать, как следствие заболеваний, хронического алкоголизма и наркомании, со снижением потребления пищи и нарушением ее усвоения.
Симптомы белково-калорийной недостаточности:
- задержка роста детей;
- слабость и потеря мышечной массы, что ведет к снижению веса тела;
- развитие обширных отеков;
- сухость и шелушение кожных покровов;
- образование медленно заживающих гноящихся язв;
- выпадение и обесцвечивание волос;
- потеря аппетита, тошнота;
- рвота с последующим обезвоживанием;
- анемия;
- снижение иммунитета.

Где его содержание больше всего, рекомендации по употреблению
Наиболее полноценные по аминокислотному составу белки содержатся в животных продуктах – мясе, рыбе, молочных продуктах, яйцах.
Достаточно белка и в крупах, макаронных изделиях, хлебе, бобовых (сое, чечевице, фасоли, бобах), в орехах и семечках.
Ниже в таблице приведена информация о том, в чем (в каких продуктах питания) содержится белок (азот).
| Продукт | Содержание белка, г/100 г продукта |
| Говядина | 20-22 |
| Свинина | 14-19 |
| Яйца | 12,7 |
| Колбасы, сосиски, сардельки | 9-14 |
| Рыба | 13-23 |
| Молоко и кисломолочные продукты | 2,6-4,3 |
| Творог | 14-18 |
| Сыр | 23-31 |
| Крупы | 7-13 |
| Хлеб | 5-8 |
| Бобовые | 22-23 |
| Овощи | 0,6-4 |
| Картофель | 2 |
| Фрукты | 0,2-2 |
| Орехи | 12-25 |
Еще больше информации о продуктах, богатых белком (азотом) в этом видео:
к оглавлению ↑Допустимо ли сочетать белковые продукты с углеводными
Следующий из системы раздельного питания запрет на совместное употребление белковых и углеводных продуктов теорией рационального питания не обосновывается, да и эволюционно человек приспособлен к потреблению смешанной пищи.
Для полноценного усвоения белка необходимо оптимальное соотношение в нем аминокислот; этому условию отвечает смешанное растительно-животное питание.
Соблюдая рекомендации по разнообразному питанию и нормам потребления белка, удается обеспечить организм достаточным количеством белка и аминокислот без приема пищевых добавок.
к оглавлению ↑Дополнительные рекомендации и советы
Помимо белков, азот включен и в состав азотсодержащих экстрактивных веществ и пуриновых оснований.

Содержащие азот экстрактивные вещества возбуждают железы желудка и способствуют лучшему усвоению белков и жиров в продуктах питания и еде.
Однако эти вещества оказывают и неблагоприятное воздействие на нервную систему, что осложняет течение болезней органов кровообращения, желудочно-кишечного тракта, почек и нервной системы.
Поэтому из диетического питания исключаются первые блюда на мясных и рыбных бульонах, жареные или тушеные вторые блюда.
Пуриновые основания нарушают обменные процессы в организме, что приводит к задержке мочевой кислоты и отложениям ее солей в тканях — основной причине подагры.
Но пуриновые основания являются также обязательным компонентом питания, и их оптимальный уровень в организме поддерживается употреблением хорошо вываренного мяса.
На Земле химический элемент азот присутствует в атмосфере, составляя большую ее часть. Азот входит в состав белков живых организмов, но они не способны усваивать атмосферный азот напрямую.
Азот поступает к ним с белковой пищей или из содержащихся в почве нитратов. В начале цепи превращения атмосферного азота в белки стоят живущие в почве бактерии рода Азотобактер.
Вконтакте
Одноклассники
Мой мир
азота | Факты, определение, использование, свойства и открытие
Азот (N) , неметаллический элемент 15 группы [Va] периодической таблицы Менделеева. Это бесцветный газ без запаха и вкуса, который является самым распространенным элементом в атмосфере Земли и является составной частью всего живого.
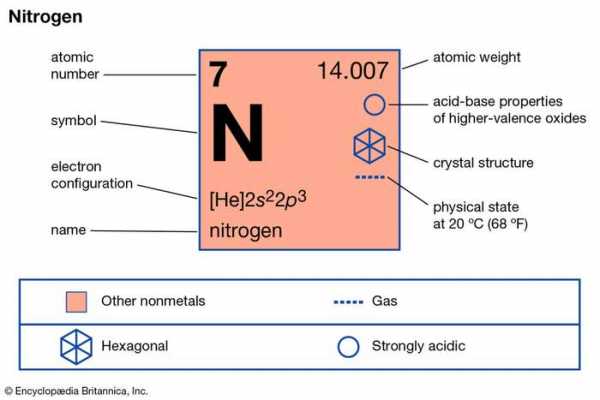 Encyclopædia Britannica, Inc.
Encyclopædia Britannica, Inc. 
Британская викторина
118 Названия и символы из таблицы Менделеева
Pu
| атомный номер | 7 |
|---|---|
| атомный вес | 14.0067 |
| точка плавления | −209,86 ° C (−345,8 ° F) |
| точка кипения | −195,8 ° C (−320,4 ° F) |
| плотность (1 атм, 0 ° C) | 1,2506 г / литр |
| обычные степени окисления | −3, +3, +5 |
| электронная конфигурация | 1 с 2 2 с 2 2 p 3 |
История
Около четырех пятых атмосферы Земли составляет азот, который был выделен и признан особенным веществом в ходе ранних исследований воздуха.Карл Вильгельм Шееле, шведский химик, показал в 1772 году, что воздух представляет собой смесь двух газов, один из которых он назвал «огненным воздухом», потому что он поддерживает горение, а другой «грязным воздухом», потому что он остался после « огненный воздух ». «Огненный воздух» - это, конечно, кислород, а «грязный воздух» - азот. Примерно в то же время азот был признан шотландским ботаником Дэниелом Резерфордом (который первым опубликовал свои открытия), британским химиком Генри Кавендишем и британским священником и ученым Джозефом Пристли, который вместе с Шееле дается заслуга в открытии кислорода.Более поздние работы показали, что новый газ является составной частью селитры, общего названия нитрата калия (KNO 3 ), и, соответственно, французский химик Жан-Антуан-Клод Шапталь в 1790 году назвал его азотом. считался химическим элементом Антуаном-Лораном Лавуазье, чье объяснение роли кислорода в горении в конечном итоге опровергло теорию флогистона, ошибочное представление о горении, которое стало популярным в начале 18 века. Неспособность азота поддерживать жизнь (по-гречески: zoe ) заставила Лавуазье назвать его азот , по-прежнему французский эквивалент азота .
Возникновение и распространение
Среди элементов азот занимает шестое место по количеству в космосе. Атмосфера Земли состоит из 75,51 процента по весу (или 78,09 процента по объему) азота; это основной источник азота для торговли и промышленности. Атмосфера также содержит различные небольшие количества аммиака и солей аммония, а также оксидов азота и азотной кислоты (последние вещества образуются во время грозы и в двигателе внутреннего сгорания).Свободный азот содержится во многих метеоритах; в газах вулканов, шахт и некоторых минеральных источников; на солнце; и в некоторых звездах и туманностях.
Азот также присутствует в минеральных отложениях селитры или селитры (нитрат калия, KNO 3 ) и чилийской селитры (нитрат натрия, NaNO 3 ), но эти отложения существуют в количествах, которые совершенно не соответствуют потребностям человека. Еще один богатый азотом материал - гуано, которое можно найти в пещерах летучих мышей и в сухих местах, часто посещаемых птицами.В сочетании азот содержится в дожде и почве в виде аммиака и солей аммония, а в морской воде - в виде аммония (NH 4 + ), нитрита (NO 2 - ) и нитрата (NO 3 ). - ) ионы. Азот составляет в среднем около 16 процентов по массе сложных органических соединений, известных как белки, присутствующих во всех живых организмах. Естественное содержание азота в земной коре составляет 0,3 части на 1000 человек. Космическое содержание - предполагаемое общее содержание во Вселенной - составляет от трех до семи атомов на атом кремния, что считается стандартом.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняИндия, Россия, США, Тринидад и Тобаго и Украина входили в пятерку крупнейших производителей азота (в форме аммиака) в начале 21 века.
Коммерческое производство и использование
Промышленное производство азота в основном осуществляется путем фракционной перегонки сжиженного воздуха. Температура кипения азота составляет -195,8 ° C (-320,4 ° F), что примерно на 13 ° C (-23 ° F) ниже, чем у кислорода, который поэтому остается позади.Азот также можно производить в больших количествах путем сжигания углерода или углеводородов в воздухе и отделения образующихся диоксида углерода и воды от остаточного азота. В небольших масштабах чистый азот получают путем нагревания азида бария, Ba (N 3 ) 2 . Различные лабораторные реакции, в результате которых образуется азот, включают нагревание растворов нитрита аммония (NH 4 NO 2 ), окисление аммиака бромной водой и окисление аммиака горячим оксидом меди.
Элементарный азот можно использовать в качестве инертной атмосферы для реакций, требующих исключения кислорода и влаги.В жидком состоянии азот имеет ценные криогенные применения; за исключением газов водорода, метана, окиси углерода, фтора и кислорода, практически все химические вещества имеют пренебрежимо малое давление пара при температуре кипения азота и поэтому существуют в виде кристаллических твердых веществ при этой температуре.
В химической промышленности азот используется для предотвращения окисления или другого порчи продукта, в качестве инертного разбавителя химически активного газа, в качестве носителя для отвода тепла или химикатов, а также в качестве ингибитора возгорания или взрывов.В пищевой промышленности газообразный азот используется для предотвращения порчи из-за окисления, плесени или насекомых, а жидкий азот используется для сублимационной сушки и для холодильных систем. В электротехнической промышленности азот используется для предотвращения окисления и других химических реакций, для создания избыточного давления в оболочках кабелей и для защиты двигателей. Азот находит применение в металлургической промышленности при сварке, пайке и пайке, где он помогает предотвратить окисление, науглероживание и обезуглероживание. В качестве инертного газа азот используется для производства вспененного или вспененного каучука, пластиков и эластомеров, в качестве газа-вытеснителя для аэрозольных баллончиков и для повышения давления жидких пропеллентов для реакционных струй.В медицине быстрое замораживание жидким азотом может использоваться для сохранения крови, костного мозга, тканей, бактерий и спермы. Жидкий азот также оказался полезным в криогенных исследованиях.
.Круговорот азота - Science Learning Hub
Азот - самый распространенный элемент в атмосфере нашей планеты. Примерно 78% атмосферы состоит из газообразного азота (N 2 ) .
Азот - важнейший компонент для всей жизни. Это важная часть многих клеток и процессов, таких как аминокислоты, белки и даже наша ДНК. Он также необходим для производства хлорофилла в растениях, который используется в фотосинтезе для производства их пищи.
В ходе этих жизненных процессов азот превращается из одной химической формы в другую.Преобразования, которые претерпевает азот при перемещении между атмосферой, землей и живыми существами, составляют круговорот азота.
Фиксация
Азот в газообразной форме (N 2 ) не может использоваться большинством живых существ. Его необходимо преобразовать или «зафиксировать» в более удобную форму с помощью процесса, называемого фиксацией. Существует три способа закрепить азот, чтобы сделать его полезным для живых существ:
- Биологически : газообразный азот (N 2 ) диффундирует в почву из атмосферы, а различные виды бактерий преобразуют этот азот в ионы аммония (NH 4 + ), которые могут использоваться заводами.Фермеры часто выращивают бобовые (например, клевер и люпин), потому что на их корнях есть клубеньки, содержащие азотфиксирующие бактерии. (Узнайте больше об этом процессе в статье «Роль клевера».)
- Сквозь молнию : Молния преобразует атмосферный азот в аммиак и нитраты (NO 3 ), которые попадают в почву с дождями.
- Промышленно : Люди научились преобразовывать газообразный азот в аммиак (NH 3 - ) и азотные удобрения для дополнения естественного фиксированного количества азота.
Разложение
Растения поглощают соединения азота корнями. Животные получают эти соединения, когда едят растения. Когда растения и животные умирают или когда животные выделяют отходы, соединения азота в органическом веществе повторно попадают в почву, где они расщепляются микроорганизмами, известными как разлагатели. В результате разложения образуется аммиак, который затем может пройти процесс нитрификации.
Нитрификация
Нитрифицирующие бактерии в почве превращают аммиак в нитрит (NO 2 - ), а затем в нитрат (NO 3 - ).Этот процесс называется нитрификацией. Такие соединения, как нитрат, нитрит, аммиак и аммоний, могут поступать из почвы растениями и затем использоваться для образования белков растений и животных.
Денитрификация
Денитрификация завершает азотный цикл путем преобразования нитрата (NO 3 - ) обратно в газообразный азот (N 2 ). Агентами этого процесса являются денитрифицирующие бактерии. Эти бактерии используют нитрат вместо кислорода при получении энергии, выделяя газообразный азот в атмосферу.
Соединения азота и потенциальное воздействие на окружающую среду
На сельское хозяйство может приходиться примерно половина фиксации азота на Земле за счет удобрений и выращивания азотфиксирующих культур. Увеличение поступления азота (в почву) привело к тому, что производится гораздо больше продуктов питания, чтобы накормить больше людей - это известно как «зеленая революция».
Однако азот, превышающий потребность растений, может вымываться из почв в водоемы. Обогащение азотом способствует эвтрофикации.
Другая проблема может возникнуть во время нитрификации и денитрификации. Когда химический процесс не завершен, может образоваться закись азота (N 2 O). Это вызывает озабоченность, поскольку N 2 O является сильнодействующим парниковым газом, способствующим глобальному потеплению.
Баланс соединений азота в окружающей среде поддерживает жизнь растений и не представляет угрозы для животных. Проблемы возникают только тогда, когда цикл не сбалансирован.
Некоторые распространенные формы азота
.Летучих органических соединений (ЛОС): ваша окружающая среда, ваше здоровье
Что такое летучие органические соединения (ЛОС)?
Летучие органические соединения (ЛОС) - это соединения, которые легко превращаются в пары или газы.
ЛОС выделяются при сжигании топлива, такого как бензин, древесина, уголь или природный газ. Их также выпускают многие товары народного потребления:
- Сигареты
- Растворители
- Краски и разбавители
- Клеи
- Принадлежности для хобби и рукоделия
- Жидкости для химической чистки
- Клей
- Консерванты для древесины
- Моющие и дезинфицирующие средства
- Репелленты от моли
- Освежители воздуха
- Строительные материалы и меблировка
- Копировальные машины и принтеры
- Пестициды
Когда ЛОС соединяются с оксидами азота в воздухе, они образуют смог.
См. Также: Загрязнение воздуха Химчистка Топливная промышленность Заправка Дома Транспортные средства и двигатели
Где находятся летучие органические соединения (ЛОС)?
- Товары народного потребления - товары для дома, строительства и хобби содержат летучие органические соединения; сигареты являются источниками ЛОС
- Воздух внутри и вне помещений: выхлопные газы транспортных средств, сигаретный и пассивный дым, а также выбросы от топлива и продуктов ЛОС
Как я могу подвергаться воздействию летучих органических соединений (ЛОС)?
Летучие органические соединения (ЛОС) обычно попадают в организм через:
Вдыхание (дыхание)
- Дыхание выхлопными газами транспортных средств, выбросами топлива, выбросами ЛОС из продуктов и процессов, содержащих ЛОС, а также сигаретным и пассивным курением
Контакт с кожей
- Прикосновение к продуктам, содержащим и выделяющим ЛОС
Что происходит, когда я подвергаюсь воздействию летучих органических соединений (ЛОС)?
Краткосрочное воздействие:
Воздействие на здоровье от летучих органических соединений может вызвать:
- Раздражение глаз и дыхательных путей
- Головные боли
- Головокружение
- Расстройства зрения
- Проблемы с памятью
Долгосрочное воздействие:
Воздействие на здоровье от летучих органических соединений может вызвать:
- Раздражение глаз, носа и горла
- Тошнота
- Усталость
- Нарушение координации
- Головокружение
- Повреждение печени, почек и центральной нервной системы
- Рак
Кто подвергается риску воздействия летучих органических соединений (ЛОС)?
- Потребители
- Многие потребительские, строительные и ремесленные товары выделяют летучие органические соединения.
- Курильщики сигарет
- Сигареты и пассивное курение являются источниками ЛОС.
- Уязвимые группы населения
- Люди с астмой, маленькие дети и пожилые люди могут быть более восприимчивы к воздействию ЛОС на здоровье.
Уменьшите риск
Если вы считаете, что воздействие летучих органических соединений повлияло на ваше здоровье, обратитесь к врачу.
Всегда тщательно мойте руки после работы с химическими веществами. В случае отравления или с вопросами о возможных ядах обращайтесь в местный токсикологический центр по телефону 1-800-222-1222.
- Вы живете в районе с проблемой смога?
- Используете ли вы принадлежности для чистки, рисования или хобби, содержащие ЛОС, подобные тем, которые указаны в приведенном выше списке примеров ЛОС?
- Вы занимаетесь химчисткой одежды или пользуетесь домашними химчистками?
- Курите ли вы или кто-либо в вашей семье табачные изделия?
- Вы используете колодезную воду?
- Удалите или уменьшите количество продуктов в вашем доме, выделяющих ЛОС.
- Используйте надлежащую вентиляцию при использовании продуктов, содержащих ЛОС.
- Храните неиспользованные химикаты в гараже или сарае.
- Утилизируйте неиспользованные химикаты надлежащим образом.
- Используйте продукты, содержащие ЛОС, в соответствии с указаниями производителя.
- По возможности используйте краски и предметы интерьера с низким содержанием ЛОС.
- Держите окна и двери открытыми, чтобы новая мебель не выделяла ЛОС и другие вредные химические вещества. Изделия из композитной древесины содержат больше ЛОС, чем изделия из цельной древесины.
- Проветрите одежду, когда забираете ее из химчистки. Достаньте одежду из полиэтиленового пакета и откройте окна или развесьте ее на улице.
- Если вы курите, бросьте. Избегайте пассивного курения, содержащего ЛОС.
- Регулярно проверяйте воду из колодца на содержание ЛОС.
- Если в вашей колодезной воде высокий уровень ЛОС, обратитесь в местное или государственное учреждение здравоохранения или в Центры по контролю и профилактике заболеваний (CDC) для получения информации о том, как снизить воздействие на вас.
- Если в вашей колодезной воде уровень ЛОС превышает рекомендуемые EPA уровни для питьевой воды, рассмотрите возможность использования бутилированной воды для питья и приготовления пищи или установки системы фильтрации с активированным углем или системы обратного осмоса.
- Храните продукты VOC в недоступном для детей месте.
Гетероциклическое соединение | химия | Британника
Гетероциклическое соединение , также называемое гетероциклом , любое из основного класса органических химических соединений, характеризующееся тем, что некоторые или все атомы в их молекулах объединены в кольца, содержащие по крайней мере один атом элемента, отличного от углерода (С). Циклическая часть (от греческого kyklos , что означает «круг») гетероциклического соединения указывает на то, что в таком соединении присутствует по крайней мере одна кольцевая структура, в то время как префикс гетеро- (от греческого гетерос , что означает «другой» или «другой» ”) Относится к неуглеродным атомам или гетероатомам в кольце.По своей общей структуре гетероциклические соединения напоминают циклические органические соединения, которые включают только атомы углерода в кольцах, например, циклопропан (с кольцом из трех атомов углерода) или бензол (с кольцом из шести атомов углерода), но наличие гетероатомов придает гетероциклическим соединениям физические и химические свойства, которые часто весьма отличаются от свойств их аналогов с полностью углеродным кольцом.
 Существует множество различных серосодержащих гетероциклов. Одним из наиболее известных является тиофен, C 4 H 4 S, производные которого встречаются в виде растительных пигментов и других природных продуктов, таких как биотин. Encyclopædia Britannica, Inc.
Существует множество различных серосодержащих гетероциклов. Одним из наиболее известных является тиофен, C 4 H 4 S, производные которого встречаются в виде растительных пигментов и других природных продуктов, таких как биотин. Encyclopædia Britannica, Inc. Гетероциклические соединения включают многие биохимические вещества, необходимые для жизни. Например, нуклеиновые кислоты, химические вещества, которые несут генетическую информацию, контролирующую наследование, состоят из длинных цепочек гетероциклических единиц, удерживаемых вместе другими типами материалов. Многие природные пигменты, витамины и антибиотики являются гетероциклическими соединениями, как и большинство галлюциногенов. Современное общество зависит от синтетических гетероциклов, используемых в качестве лекарств, пестицидов, красителей и пластмасс.
Общие аспекты гетероциклических соединений
Наиболее распространены гетероциклы с пяти- или шестичленными кольцами и гетероатомы азота (N), кислорода (O) или серы (S). Наиболее известными из простых гетероциклических соединений являются пиридин, пиррол, фуран и тиофен. Молекула пиридина содержит кольцо из шести атомов - пяти атомов углерода и одного атома азота. Каждая молекула пиррола, фурана и тиофена содержит пятичленные кольца, состоящие из четырех атомов углерода и одного атома азота, кислорода или серы соответственно.
Пиридин и пиррол представляют собой азотные гетероциклы - их молекулы содержат атомы азота наряду с атомами углерода в кольцах. Молекулы многих биологических материалов частично состоят из пиридиновых и пиррольных колец, и при сильном нагревании такие материалы дают небольшие количества пиридина и пиррола. Фактически, оба эти вещества были обнаружены в 1850-х годах в масляной смеси, образовавшейся при сильном нагревании костей. Сегодня пиридин и пиррол получают с помощью синтетических реакций. Их главный коммерческий интерес заключается в их превращении в другие вещества, главным образом в красители и лекарства.Пиридин также используется как растворитель, гидроизоляционный агент, добавка для каучука, денатурирующий спирт и добавка для окрашивания.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняФуран представляет собой кислородсодержащий гетероцикл, используемый в основном для преобразования в другие вещества (включая пиррол). Фурфурол, близкий химический родственник фурана, получают из шелухи овса и кукурузных початков и используют в производстве промежуточных продуктов для нейлона. Тиофен, гетероцикл серы, по своим химическим и физическим свойствам напоминает бензол.Это частый загрязнитель бензола, полученного из природных источников, и он был впервые обнаружен во время очистки бензола. Как и другие соединения, он используется в основном для преобразования в другие вещества. Фуран и тиофен были открыты во второй половине 19 века.
В целом, физические и химические свойства гетероциклических соединений лучше всего понять, сравнивая их с обычными органическими соединениями, не содержащими гетероатомов.
.