Продукты содержащие аммиак
| Спецификация: | Yellow line Roche Diagnostics Аммиак | Enzytec™ Liquid Аммиак |
| Количество определений: | 50 (проба, бланк или стандартный раствор) | 4×10 (проба, бланк или стандартный раствор) |
| Стандарт: | раствор аммиака (концентрация указана на этикетке флакона) | не входит в набор |
| Длина волны: | 340 нм, 334 нм или 365 нм | 340 нм, 334 нм или 365 нм |
| Матрицы: | пиво, соки, молоко, хлебобулочные изделия, мясные изделия, сыр, продукты из лакрицы | пиво, соки, молоко, хлебобулочные изделия, мясные изделия, сыр, продукты из лакрицы |
| Пробоподготовка: | при необходимости: разбавление, фильтрование, обесцвечивание, нейтрализация, измельчение, гомогенизация, депротеинизация, обезжиривание | при необходимости: разбавление, фильтрование, обесцвечивание, нейтрализация, измельчение, гомогенизация, депротеинизация, обезжиривание |
| Длительность анализа: | 25 минут | 30 минут |
| Специфичность: | аммиак | аммиак |
| Предел обнаружения: | 0,08 мг/л | 0,3 мг/л |
| Стандарты, методы: | ГОСТ 32939-2014, MEBAK, LFGB | СОП производителя |
аммиака | Определение и использование
Аммиак (NH 3 ) , бесцветный едкий газ, состоящий из азота и водорода. Это простейшее стабильное соединение из этих элементов и служит исходным материалом для производства многих коммерчески важных соединений азота.
Аммиак и амины имеют слегка уплощенную треугольную пирамидальную форму с неподеленной парой электронов над азотом. В ионах четвертичного аммония эту область занимает четвертый заместитель. Encyclopædia Britannica, Inc.Использование аммиака
Аммиак используется в основном в качестве удобрения. В Соединенных Штатах его обычно наносят прямо на почву из резервуаров, содержащих сжиженный газ. Аммиак также может быть в форме солей аммония, таких как нитрат аммония, NH 4 NO 3 , сульфат аммония (NH 4 ) 2 SO 4 и различные фосфаты аммония. Мочевина, (H 2 N) 2 C = O, является наиболее часто используемым источником азота для удобрений во всем мире.Аммиак также используется в производстве коммерческих взрывчатых веществ (например, тринитротолуола [TNT], нитроглицерина и нитроцеллюлозы).
В текстильной промышленности аммиак используется при производстве синтетических волокон, таких как нейлон и вискоза. Кроме того, он используется для окрашивания и чистки хлопка, шерсти и шелка. Аммиак служит катализатором при производстве некоторых синтетических смол. Что еще более важно, он нейтрализует кислотные побочные продукты нефтепереработки, а в резиновой промышленности предотвращает коагуляцию необработанного латекса во время транспортировки с плантации на фабрику.Аммиак также находит применение как в аммиачно-содовом процессе (также называемом процессом Сольве), широко используемом методе производства кальцинированной соды, так и в процессе Оствальда, способе превращения аммиака в азотную кислоту.
Аммиак используется в различных металлургических процессах, включая азотирование листов сплава для упрочнения их поверхностей. Поскольку аммиак легко разлагается с образованием водорода, он является удобным портативным источником атомарного водорода для сварки. Кроме того, аммиак может поглощать значительное количество тепла из окружающей среды (т.е.е., один грамм аммиака поглощает 327 калорий тепла), что делает его полезным в качестве хладагента в холодильном оборудовании и оборудовании для кондиционирования воздуха. Наконец, среди его второстепенных применений - включение в некоторые бытовые чистящие средства.
Получите эксклюзивный доступ к контенту нашего 1768 First Edition с подпиской. Подпишитесь сегодняПолучение аммиака
Чистый аммиак был впервые получен английским ученым-физиком Джозефом Пристли в 1774 году, а его точный состав был определен французским химиком Клод-Луи Бертолле в 1785 году.Аммиак неизменно входит в пятерку основных химических веществ, производимых в США. Основным промышленным методом производства аммиака является процесс Габера-Боша, который включает прямую реакцию элементарного водорода и элементарного азота. № 2 + 3H 2 → 2NH 3
Эта реакция требует использования катализатора, высокого давления (100–1000 атмосфер) и повышенной температуры (400–550 ° C [750–1020 ° F]). Фактически, равновесие между элементами и аммиаком способствует образованию аммиака при низкой температуре, но для достижения удовлетворительной скорости образования аммиака требуется высокая температура.Можно использовать несколько разных катализаторов. Обычно катализатор представляет собой железо, содержащее оксид железа. Однако как оксид магния на оксиде алюминия, который был активирован оксидами щелочных металлов, так и рутений на угле использовались в качестве катализаторов. В лаборатории аммиак лучше всего синтезировать путем гидролиза нитрида металла. Mg 3 N 2 + 6H 2 O → 2NH 3 + 3Mg (OH) 2
Физические свойства аммиака
Аммиак - бесцветный газ с резким резким запахом.Его точка кипения составляет -33,35 ° C (-28,03 ° F), а температура замерзания -77,7 ° C (-107,8 ° F). Он имеет высокую теплоту испарения (23,3 килоджоулей на моль при его температуре кипения), и с ним можно обращаться как с жидкостью в теплоизолированных контейнерах в лаборатории. (Теплота испарения вещества - это количество килоджоулей, необходимое для испарения одного моля вещества без изменения температуры.) Молекула аммиака имеет форму тригональной пирамиды с тремя атомами водорода и неподеленной парой электронов, прикрепленных к атом азота.Это полярная молекула, которая тесно связана из-за сильной межмолекулярной водородной связи. Диэлектрическая проницаемость аммиака (22 при -34 ° C [-29 ° F]) ниже, чем у воды (81 при 25 ° C [77 ° F]), поэтому он является лучшим растворителем для органических материалов. Однако он все еще достаточно высок, чтобы аммиак мог действовать как умеренно хороший ионизирующий растворитель. Аммиак также самоионизируется, хотя и в меньшей степени, чем вода. 2NH 3 ⇌ NH 4 + + NH 2 -
Химическая активность аммиака
Аммиак сгорает с трудом, но образует газообразный азот и воду.4NH 3 + 3O 2 + тепло → 2N 2 + 6H 2 O Однако при использовании катализатора и при правильных температурных условиях аммиак реагирует с кислородом с образованием оксида азота NO, который окисляется до диоксида азота NO 2 и используется в промышленном синтезе азотной кислоты.
Аммиак легко растворяется в воде с выделением тепла. NH 3 + H 2 O ⇌ NH 4 + + OH - Эти водные растворы аммиака являются основными и иногда их называют растворами гидроксида аммония (NH 4 OH).Однако равновесие таково, что 1,0-молярный раствор NH 3 дает только 4,2 миллимоля гидроксид-иона. Гидраты NH 3 · H 2 O, 2NH 3 · H 2 O и NH 3 · 2H 2 O существуют и, как было показано, состоят из молекул аммиака и воды, связанных межмолекулярными связями. водородные связи.
Аммиак жидкий широко используется в качестве неводного растворителя. Щелочные металлы, а также более тяжелые щелочноземельные металлы и даже некоторые внутренние переходные металлы растворяются в жидком аммиаке, образуя синие растворы.Физические измерения, включая исследования электропроводности, доказывают, что этот синий цвет и электрический ток связаны с сольватированным электроном. металл (рассеянный) ⇌ металл (NH 3 ) x ⇌ M + (NH 3 ) x + e - (NH 3 ) y Эти растворы являются отличными источниками электронов для восстановления других химических соединений. По мере увеличения концентрации растворенного металла раствор становится более глубокого синего цвета и, наконец, превращается в раствор цвета меди с металлическим блеском.Электропроводность уменьшается, и есть свидетельства того, что сольватированные электроны объединяются с образованием электронных пар. 2 e - (NH 3 ) y ⇌ e 2 (NH 3 ) y Большинство солей аммония также легко растворяются в жидком аммиаке.
.Последние разработки процесса удаления аммиака для очистки промышленных сточных вод
Следует отметить, что загрязнение сточных вод аммиачным азотом, как сообщается, представляет большую угрозу для окружающей среды. В этом традиционном методе устранения загрязнения сточными водами аммиачным азотом применяется технология башни с уплотненным слоем. Тем не менее, эта технология, похоже, создает несколько проблем с приложениями. На протяжении многих лет исследователи тестировали различные типы процессов очистки от аммиака, чтобы преодолеть недостатки традиционной технологии очистки от аммиака.В этом направлении в настоящем исследовании подчеркивается недавнее развитие процесса очистки промышленных сточных вод от аммиака. Кроме того, в этом исследовании рассматривается применение очистки от аммиака для различных типов промышленных сточных вод и некоторых важных рабочих параметров. Кроме того, в этой статье обсуждаются некоторые вопросы, связанные с обычным отпарным аппаратом аммиака для промышленной очистки. Наконец, это исследование объясняет будущие перспективы метода очистки от аммиака. Таким образом, этот обзор способствует повышению эффективности очистки от аммиака и его применению для очистки промышленных сточных вод.
1. Введение
Деятельность человека, по-видимому, является основным источником загрязнения воды, например, сельскохозяйственная, промышленная и муниципальная деятельность. Было доказано, что избыток азота, попадающий в окружающую среду, оказывает негативное влияние на качество воды, здоровье человека и экосистемы [1]. Тем не менее, доступен широкий спектр технологий для уменьшения выбросов аммиачного азота в окружающую среду, таких как отгонка аммиака [2], хлорирование до точки останова [3], ионный обмен [4], электродиализ [5] и биологическая нитрификация [6]. ].Метод очистки от аммиака имеет несколько плюсов, так как это относительно простой и экономичный процесс удаления аммиака из сточных вод [7]. Кроме того, ценный аммиак, очищенный от сточных вод, может быть восстановлен в процессе очистки. Из-за стабильности этого процесса, процесс очистки от аммиака считается подходящим методом очистки сточных вод, содержащих высокие концентрации аммиака и токсичных соединений [8]. Следовательно, отгонка аммиака стала предметом пристального внимания исследователей и промышленного сообщества.Таким образом, были проведены многочисленные лабораторные и экспериментальные исследования, особенно для широкого спектра промышленных сточных вод, требующих рентабельного восстановления.
В этой статье рассматриваются несколько возникающих вопросов, связанных с восстановлением аммиачного азота с использованием метода отпарки аммиака, а также некоторые важные рабочие параметры. Кроме того, в этой статье рассматривается недавний прогресс в методе отгонки аммиака с использованием усовершенствованных газожидкостных контакторов, проведенный некоторыми исследователями.Затем было проведено сравнение усовершенствованных жидкостных контакторов и традиционной насадочной башни. Наконец, в этой статье исследуются будущие перспективы этого процесса очистки от аммиака.
2. Процесс удаления аммиака
Процесс удаления аммиака основан на принципе массопереноса. Это процесс, при котором сточные воды контактируют с воздухом для удаления газообразного аммиака, присутствующего в сточных водах. Аммиак в сточных водах может быть двух видов: ионы аммония и газообразный аммиак.Относительные концентрации газообразного аммиака и ионов аммония зависят от pH и температуры сточных вод [9]. Образованию газообразного аммиака способствует увеличение pH, что смещает химическое равновесие вправо, вызывая образование газообразного аммиака. Поскольку для эффективного удаления аммиака требуется высокий pH, известь используется для увеличения значений pH сточных вод перед отпаркой аммиака [9]. Фактически, для восстановления различных типов сточных вод, содержащих аммиачный азот, применялись различные типы конфигураций процесса отгонки аммиака.Например, O’Farell et al. провели исследование по удалению азота путем отгонки вторичных стоков муниципальных очистных сооружений [10]. На рисунке 1 представлена схематическая диаграмма процесса осаждения извести и процесса отпаривания аммиака. Известь добавляется для повышения pH входящего потока перед отгонкой, после чего следует процесс повторной карбонизации для нейтрализации. Помимо повышения pH сточных вод, оксид кальция (известь) генерирует карбонат кальция в сточных водах и служит коагулянтом для твердых и твердых частиц.Кроме того, O’Farell et al. обнаружили, что метод отгонки аммиака может удалить до 90% аммиака из вторичных стоков [10].
Между тем Raboni et al. исследовали эффективность метода очистки от аммиака для восстановления подземных вод, загрязненных фильтратом [11] (Рисунок 2). В исследовании добавляли полиэлектролит, гидроксид натрия и хлорид железа (iii) для процессов коагуляции-флокуляции и седиментации при pH выше 11 [11].Система также включала нагреватель для нагрева сточных вод до 38 ° C и регенерацию аммиака путем абсорбции серной кислотой. Наконец, сточные воды нейтрализовали после добавления серной кислоты. В результате они обнаружили, что система очистки от аммиака для подземных вод, загрязненных фильтратом, показала эффективность удаления 95,4% при начальной концентрации аммиака 199,0 мг / л.
Затем Саракко и Генон исследовали производительность системы воздушной десорбции для очистки аммиачного азота из промышленных стоков (рис. 3) [12].Они предположили, что этот способ возможен только в том случае, если промышленные сточные воды будут характеризоваться относительно высокой температурой и концентрацией аммиака. За процессом отгонки следовали процессы абсорбции и кристаллизации. Саракко и Генон пришли к выводу, что отгонка аммиака и система регенерации, наряду с его внутренним рециркуляцией воздуха, были технически осуществимы и просты в управлении [12].
3. Применение отгонки аммиака при очистке промышленных сточных вод
На сегодняшний день пилотные установки по отгонке аммиака используются для очистки различных типов сточных вод, содержащих высокие концентрации аммиака и токсичных соединений, например, образующихся из вторичных сточных вод городских очистные сооружения [10], навоз животных [13] и фильтрат со свалок [14].Совсем недавно очистка сточных вод после анаэробного сбраживания применялась к очистке от аммиака, поскольку этот метод имеет как экономические, так и экологические преимущества. Биогаз, полученный в результате анаэробного сбраживания, использовался для удаления аммиака, чтобы предотвратить ингибирование метаногенеза в анаэробном реакторе [15–17]. Между тем, Бонмати и Флотатс показали, что для удаления аммиака из свиного навоза не требуется модификации pH [18]. С другой стороны, Limoli et al. исследовали удаление аммиака из сброженного навоза сырого навоза с помощью процесса отгонки при турбулентном перемешивании.Они обнаружили, что процесс удаления аммиака посредством турбулентного перемешивания действительно возможен для дигестата сырого навоза [19].
Таблица 1 показывает, что метод удаления аммиака действительно очень эффективен при очистке сточных вод, содержащих аммиачный азот, токсичными соединениями. Кроме того, отгонка аммиака в сочетании с анаэробным сбраживанием, по-видимому, повышает эффективность процесса анаэробного сбраживания, помимо того, что удаление аммиака является рентабельным. Тем не менее, Серна-Маза и др. показали, что отгонка аммиака на месте в мезофильных условиях вряд ли будет иметь какое-либо коммерческое применение для отходов с промежуточными концентрациями общего аммиачного азота, поскольку только отгонка с высокой общей концентрацией аммиачного азота смогла снизить общую концентрацию аммиачного азота ниже более высокого порога ингибирования, составляющего приблизительно 8 г · Н · л -1 [29].Таким образом, отгонка в сочетании с разбавлением может быть лучшим средством контроля общей концентрации аммиачного азота. Затем Collivignarelli et al. обнаружили, что отгонка аммиака без дозировки подщелачивающего вещества была возможна, когда начальная щелочность фильтрата была равна кислотности удаляемых ионов аммония или превышала ее [30]. Примечательно, что это потенциально может минимизировать использование химикатов и снизить эксплуатационные расходы на удаление аммиачного азота из фильтрата. Отгонка аммиака также представляется эффективной и подходящей для сельского хозяйства благодаря простоте процесса и рентабельности при эффективном удалении аммиака.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
4.Условия процесса
Многочисленные исследования выявили влияние различных рабочих параметров на производительность процесса очистки от аммиака. Некоторые важные параметры, которые, как сообщается, влияют на эффективность отгонки аммиака, - это температура, pH и соотношение воздуха и воды.
4.1. Температура
Доказано, что температура оказывает значительное влияние на производительность отпарной колонны аммиака. Это связано с тем, что растворимость аммиака в воде регулируется законом Генри.В законе Генри постоянная газа зависит от растворенного вещества, растворителя и температуры [31]. Например, Campos et al. обнаружил, что удаление аммиака из фильтрата полигона при 60 ° C было относительно значительным в течение 7 часов, чем при 25 ° C [32]. Как правило, более эффективное удаление аммиака может быть достигнуто при более высокой температуре. Саракко и Генон также обнаружили, что капитальные затраты на отпарную колонну аммиака при температуре отпарки 80 ° C были вдвое меньше, чем при 40 ° C. Тем не менее, с экономической точки зрения, повышение температуры может привести к увеличению стоимости предварительного нагрева [12].
4.2. pH
Аммиачный азот в воде находится в равновесии между молекулярной (NH 3 ) и ионной формой (NH 4 + ) в соответствии со следующей реакцией:
Распределение между молекулярным аммиаком и ионами аммония в воде может определяется формулами (2) [16] и (3) [18]:
где - концентрация молекулярного аммиака, - общая концентрация аммиака, - концентрация ионов водорода и - константа кислотной ионизации.Кроме того, можно выразить через температуру, как показано в (3). Более высокий pH способствует образованию газообразного аммиака, тогда как более низкий pH способствует образованию ионов аммония. Следовательно, повышение уровня pH сточных вод перед отгонкой аммиака имеет решающее значение для содействия образованию молекулярного аммиачного азота для отгонки. Однако, согласно Идальго и др., Чрезмерное повышение pH приводит к дополнительным затратам на известь, что невозможно с точки зрения затрат. Следовательно, для достижения баланса между эффективностью процесса и экономическими затратами требуется оптимальный pH.Они обнаружили, что, когда pH превышал 10,5, эффективность удаления была незначительной, потому что pH больше не влиял на ионизационный баланс между молекулярным аммиаком и ионным аммонием, но понесенные затраты значительно выросли из-за дополнительного расхода извести, необходимого для повышения уровня pH [33] . Между тем, Markou et al. выявили незначительное влияние используемых типов щелочей (гидроксид калия, гидроксид натрия и гидроксид кальция) на эффективность удаления аммиака [34]. Однако кальциевая щелочь была предпочтительнее из-за снижения содержания твердых частиц, концентрации тяжелых металлов и цвета сточных вод [35].
4.3. Отношение воздуха к воде
Отношение воздуха к воде - важный параметр, который влияет на скорость удаления аммиака из воды. На массоперенос аммиака в воздух влияет разница между уровнем концентрации аммиака в жидкой форме и в воздушной фазе [18]. Lei et al. обнаружил, что на эффективность удаления аммиака анаэробных стоков влияет соотношение воздух / вода. Исследование показало, что более высокая скорость удаления аммиака была достигнута через 12 часов при скорости воздушного потока 10 л / мин по сравнению со скоростью воздушного потока при 3 л / мин и 5 л / мин [16].Тем не менее, с инженерной точки зрения Lei et al. пришли к выводу, что 5 л / мин на 1 л анаэробных стоков должно быть осуществимо из-за дорогостоящего метода использования скорости воздушного потока 10 л / мин на 1 л сточных вод с увеличением эффективности удаления всего на 5% по сравнению с расходами воздуха из От 5 л / мин до 10 л / мин [16]. Затем Campos et al. показали, что влияние соотношения воздуха и воды на производительность отгонки аммиака при более высокой температуре было менее значительным, поскольку это приводило к удалению аммиака более 91% при 60 ° C со скоростью воздушного потока от 73 до 120 л / ч [32] .
5. Проблемы, связанные со сточными водами отпарной колонны аммиака при промышленной очистке
Процесс отпарки аммиака успешно применялся для многих типов сточных вод с высоким содержанием аммиака (Таблица 1). Метод относится к методу, который контролируется и не изменяется токсичными соединениями. Тем не менее, процесс отгонки аммиака имеет несколько недостатков. Среди вопросов, связанных с внедрением отпарной колонны аммиака для удаления аммиачного азота из сточных вод, являются проблемы загрязнения, образование шлама и выброс газообразного аммиака.
5.1. Проблемы засорения
Проблемы засорения в колонне отпарной колонны аммиака вызваны образованием накипи карбоната кальция на поверхности упаковочных материалов. Накипь накапливается на упаковочных материалах, что снижает эффективность зачистки [32]. Виотти и Гаваши обнаружили, что постепенное масштабирование насадки снизило эффективность отпарной колонны с 98% до 80% после 6 месяцев эксплуатации. Образование отложений карбоната кальция на упаковочном материале происходит из-за абсорбции диоксида углерода из воздушного потока, используемого для отгонки.Причем природа карбоната кальция варьируется от мягкой до твердой. Таким образом, Виотти и Гаваши предложили химическую очистку для более эффективного удаления аммиака из сточных вод [36]. Высокие затраты на эксплуатацию и техническое обслуживание воздушной десорбции можно объяснить образованием отложений карбоната кальция [37].
5.2. Производство осадка
Очищенный сток после отпарки аммиака часто не соответствует стандартам сброса. Образование большого количества шлама и сточных вод с высокой щелочностью, связанных с отгонкой аммиака, приводят к дополнительным затратам на обработку этого процесса.Однако карбонат кальция из шлама отпарной колонны аммиака может быть извлечен. Мари и Звинованда, например, использовали технику флотации для извлечения карбоната кальция из осадка сточных вод [38]. В результате они обнаружили, что технология флотации потенциально может извлекать известняк технического качества из ила сточных вод [38]. Между тем, He et al. оценили осуществимость и повышение эффективности очистки сточных вод, очищенных от щелочи, в вентилируемых построенных водно-болотных угодьях [39].Построенное водно-болотное угодье было относительно простым и оснащено экологически чистыми технологиями, позволяющими выдерживать сточные воды с экстремальным pH. He et al. также обнаружили, что очистка щелочных стоков была осуществима из-за высокой буферной способности водно-болотных угодий [39].
5.3. Аммиачный газ
Процесс удаления аммиака приводит к выбросу аммиака в окружающую среду, что вызывает дополнительные экологические проблемы. Извлечение аммиака путем абсорбции обычно используется для предотвращения прямого выброса газообразного аммиака в окружающую среду.Ferraz et al. использовали серную кислоту для извлечения очищенного аммиака из фильтрата полигона и показали, что было извлечено 87% очищенного аммиака [22]. Затем Zhu et al. обнаружил, что при оптимальных условиях pH 12, скорости воздушного потока 0,50 м 3 / ч, температуре 60 ° C и времени очистки 120 мин; 0,2 моль / л серной кислоты может абсорбировать примерно 93% аммиака, очищенного от объема сточных вод после очистки ацетилена [25]. Между тем, Laureni et al. пришли к выводу, что удаление аммиака в сочетании с абсорбцией оказалось возможным вариантом повышения ценности азота, содержащегося в навозе свиней.Побочным продуктом этого процесса был сульфат аммония, который является товарным продуктом в сельском хозяйстве в качестве удобрений [15].
6. Достижения в процессе очистки от аммиака
Исследования по повышению эффективности очистки от аммиака не ослабевают. Недавние разработки по удалению аммиака путем отгонки аммиака включают следующее: модификации реактора отгонки аммиака, мембранный контактор, мембранная дистилляция, цикл ионообменной отгонки и отгонка аммиака с помощью микроволн.
6.1. Модификации реактора отпарки аммиака
Строительство конкретного реактора отпарки аммиака имеет решающее значение, поскольку оно оказывает сильное влияние на общую эффективность очистки и капитальные затраты. В обычном реакторе отгонки аммиака используется технология насадочной колонны, в которой насадочные материалы используются для улучшения массопереноса между двумя фазами. Башня с противоточным наполнением втягивает воздух через свои отверстия внизу, когда сточные воды перекачиваются в верхнюю часть колонны с набивкой.Тем не менее, в результате этого процесса на поверхности упаковочных материалов образуются карбонатные отложения, которые со временем могут влиять на эффективность удаления аммиака. Кроме того, средняя глубина башни с насадочным слоем может составлять от 6,1 до 7,6 метров, что требует значительного пространства. Поэтому некоторые исследователи предложили использовать инновационные реакторы отгонки аммиака в качестве решения для эффективного удаления аммиака. Среди предложенных инновационных реакторов для отгонки аммиака были вращающийся насадочный слой [40], барботажный реактор-аэроциклон [41] и полупериодический струйный петлевой реактор [42].
6.1.1. Полупериодический струйный петлевой реактор
Удаление аммиака посредством десорбции воздухом в полупериодическом струйном петлевом реакторе было инициировано Degermenci et al., В котором аммиак удаляется струйным петлевым реактором, чтобы снизить затраты на строительство и эксплуатационные расходы при обычной отпарке аммиака процесс. Он также имеет более высокий коэффициент массопередачи и более простую адаптацию от пилотного к промышленному масштабу [42]. Струйный реактор с циркуляцией обычно применялся для химических или биохимических каталитических реакций [43].Струйный реактор с циркуляцией обеспечивает исключительные характеристики перемешивания при относительно низком потреблении энергии для применений, связанных с переносом массы [44].
Общий обзор струйного реактора с контуром проиллюстрирован на рисунке 4. В целом реакторы с струйным контуром были сконструированы во многих конструкциях с точки зрения устройства, размеров сопла, вытяжной трубы и положения входа струйной струи [45]. Принцип струйного петлевого реактора заключается в использовании кинетической энергии высокоскоростной струи жидкости для увлечения газовой фазы, помимо создания тонкой дисперсии между газовой и жидкой фазами [46].
Degermenci et al. разработали (4) для моделирования скорости удаления аммиака методом воздушной десорбции в струйном реакторе с циркуляцией [42].
.нуклеофильного замещения - галогеноалканы и аммиак
На второй стадии реакции молекула аммиака может удалить один из атомов водорода -NH 3 + . Ион аммония образуется вместе с первичным амином - в данном случае этиламином.
Однако эта реакция обратима. Таким образом, ваш продукт будет содержать смесь ионов этиламмония, аммиака, этиламина и ионов аммония. Вашим основным продуктом будет этиламин, только если аммиак присутствует в очень большом избытке.
К сожалению, на этом реакция не заканчивается. Этиламин является хорошим нуклеофилом и атакует неиспользованный бромэтан. Это настолько сложно, что рассматривается на отдельной странице. Вы найдете ссылку внизу этой страницы.
Реакция третичных галогеноалканов с аммиаком
Факты
Факты реакций точно такие же, как и с первичными галогеноалканами. Галогеноалкан нагревают в герметичной пробирке с раствором аммиака в этаноле.
Например:
Следуют:
Механизм
Этот механизм включает начальную ионизацию галогеноалкана:
с последующей очень быстрой атакой аммиака на образовавшийся карбокатион (ион карбония):
Это снова пример нуклеофильной замены .
На этот раз в медленной стадии реакции участвует только один вид - галогеноалкан.Она известна как реакция S N 1.
Есть вторая стадия точно так же, как с первичными галогеноалканами. Молекула аммиака удаляет ион водорода из группы -NH 3 + в обратимой реакции. Ион аммония образуется вместе с амином.
Реакция вторичных галогеноалканов с аммиаком
Маловероятно, что какой-либо из действующих в Великобритании учебных программ для 16–18-летних спросит вас об этом.В крайне маловероятном случае, когда он вам когда-либо понадобится, вторичные галогеноалканы используют и , и механизм S N 2, и механизм S N 1.
Убедитесь, что вы понимаете, что происходит с первичными и третичными галогеноалканами, а затем при необходимости адаптируйте это для вторичных.
-
Куда бы вы сейчас хотели отправиться?
-
Помогите! Расскажите мне об этих механизмах.. .
Чтобы посмотреть на дальнейшее замещение в этих реакциях. . .
В меню реакций нуклеофильного замещения. . .
В меню других типов механизмов. . .
В главное меню. . .
ПРОМЫШЛЕННОСТЬ АММИАКА

Fertilizers Europe опубликовала в конце 2018 года важный отчет, в котором исследуются ключевые движущие силы индустрии удобрений и описываются «вероятные события, ожидаемые в период до 2030 года». Эти разработки включают производство «возможно 10%» европейского аммиака из возобновляемой электроэнергии с использованием электролизеров для производства возобновляемого водородного сырья. Это потребует увеличения мощности по производству зеленого аммиака до более чем миллиона тонн в год в течение десяти лет.
В отчете Feeding Life 2030 также описывается политическая основа, необходимая для «поддержания Видения». В этом видении аммиак находится «на перекрестке питания и энергии» и признан «недостающим звеном» в грядущей трансформации энергии ».
Подробнее
Один из самых интересных вопросов, оставшихся без ответа, относительно зеленого аммиака: а как насчет мочевины?
В прошлом месяце крупное заявление компании Stamicarbon («мировой лидер в области проектирования, лицензирования и разработки установок по производству карбамида») предполагает ответ: в долгосрочном контексте изменения климата использование мочевины в качестве удобрения, возможно, просто необходимо поэтапно внедрить. вне.
Stamicarbon объявил о своей новой программе инноваций на мероприятии «День будущего» в Утрехте в апреле. Его инновационная программа охватывает три области: специальные удобрения, цифровизация и «Возобновляемое производство удобрений (использование энергии ветра или солнца для производства удобрений)».
Подробнее

Haldor Topsoe значительно улучшил краткосрочные перспективы экологически чистого аммиака, объявив о демонстрации своей установки для синтеза аммиака нового поколения.В этой технологии используется твердооксидная электролизная ячейка для производства синтез-газа (водорода и азота), который питает существующую технологию Haldor Topsoe: завод Haber-Bosch. Продукт представляет собой аммиак, полученный из воздуха, воды и возобновляемой электроэнергии.
Проект "SOC4Nh4" недавно получил финансирование от Датского энергетического агентства, что позволило Haldor Topsoe продемонстрировать систему со своими академическими партнерами и подготовить технико-экономическое обоснование для небольшой экспериментальной установки по производству зеленого аммиака в промышленных масштабах, которую она надеется построить. к 2025 г.У этой технологии есть два аспекта, которые делают ее настолько важной: надежность и эффективность.
Подробнее

На этой неделе Yara объявила о значительном прогрессе в производстве «зеленого аммиака» на своем заводе в Пилбаре, Австралия. Его новым партнером в этом проекте является ENGIE, глобальная группа по энергетике и услугам, которая в прошлом году взяла на себя серьезное обязательство по развитию крупномасштабных проектов по возобновляемым водородам.
Я впервые сообщил о планах Yara по демонстрации солнечного аммиака на заводе в Пилбара в сентябре 2017 года.Объявление на этой неделе означает, что проект Pilbara перешел на следующий этап технико-экономического обоснования. Тем не менее, основные элементы проекта уже были спроектированы и построены: во время планового ремонта в прошлом году для технического обслуживания завода была завершена врезка водородного трубопровода, а это означает, что установка Haber-Bosch готова напрямую получать водород, как только Электролизер построен для снабжения его возобновляемым сырьем.
Подробнее
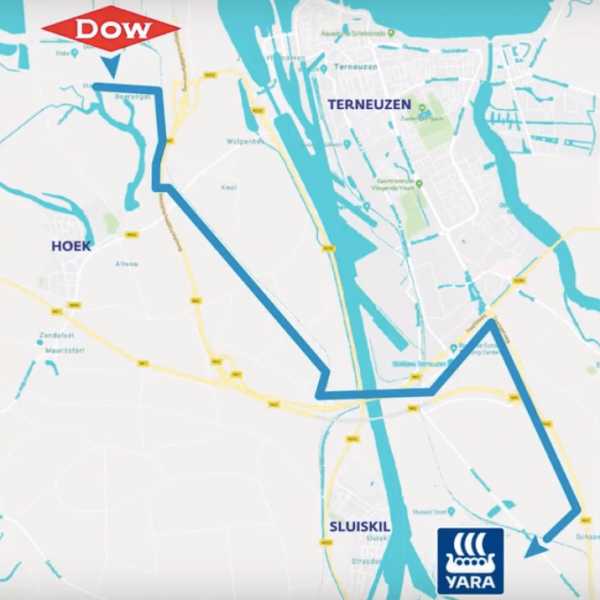
В прошлом году компания Yara Sluiskil в Нидерландах модернизировала свой существующий завод по производству аммиака, подключив водородный трубопровод, тем самым снизив свою зависимость от ископаемого топлива.Трубопровод был введен в эксплуатацию в октябре 2018 года и теперь «обеспечивает эффективную и безопасную транспортировку водорода», который ранее являлся отходом на соседней установке крекинга этилена Dow. Уже сейчас проект «обеспечивает сокращение выбросов CO2 на 10 000 тонн» и снижение энергопотребления на «0,15 петаджоулей (ПДж) в год».
Это, возможно, первая модернизация установки по обезуглероживанию аммиака, и она показывает, что сокращение выбросов от существующих установок по производству аммиака сегодня возможно и доступно.
Подробнее

Mission Possible , крупный отчет, опубликованный в конце 2018 года, делает вывод о том, что декарбонизация производства аммиака к 2050 году технически и экономически осуществима. Среди 172 страниц предположений, анализа и объяснений, Mission Possible исследует пути производства и рынки зеленого аммиака и его производных зеленых азотных удобрений. В нем рассматривается относительно простой вопрос о том, как заменить ископаемое сырье возобновляемым водородом для синтеза аммиака, а также более сложный вопрос о том, как получить или заменить молекулы диоксида углерода, содержащиеся в мочевине, наиболее распространенном азотном удобрении.
Экономические выводы отчета не удивят никого, кто занимается производством аммиака или политикой. Да, зеленый аммиак в настоящее время дороже ископаемого аммиака, хотя это ненадолго. И нет, «ни одно из повышений цен для конечных потребителей не является достаточно большим, чтобы служить аргументом против жесткой политики, направленной на декарбонизацию».
Подробнее

В конце 2018 года JGC Corporation выпустила пресс-релиз, посвященный «первому в мире» производству аммиака, продемонстрировав на своем пилотном заводе в Корияме как «синтез аммиака с водородом, полученным путем электролиза воды с помощью возобновляемых источников энергии, так и производство электричество через газовые турбины, работающие на синтезированном аммиаке.«
Демонстрируя возможность использования аммиака по обе стороны уравнения возобновляемой энергии - во-первых, производство зеленого аммиака из периодически возобновляемых источников электроэнергии и, во-вторых, сжигание этого безуглеродного топлива для выработки электроэнергии - проект демонстрирует роль аммиака в «создание энергетической цепочки ... которая не выделяет CO2 (без CO2) от производства до производства электроэнергии».
Подробнее
ЭТО ОБНОВЛЕНИЕ ДОСТУПНО ТОЛЬКО ДЛЯ ЧЛЕНОВ САЙТА
В августе 2018 года агентство Reuters сообщило, что дешевый природный газ стимулировал развитие отрасли по всей Альберте, и сообщило, что CF Industries увеличивает производство аммиака на своем заводе в Medicine Hat.
Подробнее
.